题目内容
14.下列图象分别表示有关反应的反应过程与能量变化的关系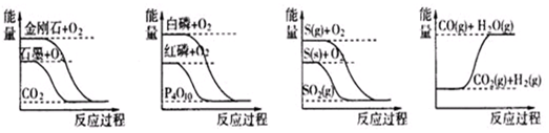
据此判断下列说法中正确的是( )
| A. | 石墨转变为金刚石是吸热反应 | |
| B. | 相同条件下,白磷比红磷稳定 | |
| C. | 相同条件下,等质量S(g)和S (s)的能量比较,S (s)能量较高 | |
| D. | CO(g)+H2O(g)=CO2(g)+H2 (g)是吸热反应 |
分析 A.由图可知,金刚石的能量高于石墨的能量;
B.由图可知,生成物相同,反应物中白磷能量高于红磷能量;
C.生成物相同,反应物中气态S的能量大于固态S的能量;
D.由图可知,CO2(g)、H2(g)的总能量小于CO(g)、H2O(g)的总能量.
解答 解:A.图象分析金刚石能量高于石墨,石墨转变为金刚石是吸热反应,故A正确;
B.由图可知,生成物相同,反应物中白磷能量高于红磷能量,则红磷比白磷稳定,故B错误;
C.依据图象分析固体硫变化为气态硫需要吸收能量,相同条件下,等质量S(g)和S(s)的能量比较,S(s)较小,故C错误;
D.由图象可知该反应是能量升高的反应,CO2(g)+H2(g)是反应物,CO(g)+H2O(g)是生成物,为吸热反应,所以反应方程为CO2(g)+H2(g)=CO(g)+H2O(g)△H>0,所以其逆反应的△H<0,为放热反应,故D错误.
故选A.
点评 本题综合考查能量变化知识,为高频考点,侧重学生的分析能力的考查,注意对放热反应和吸热反应的理解和掌握,难度不大.

练习册系列答案
相关题目
13.下列关于电解质溶液的叙述正确的是( )
| A. | 常温下,c(NH4+)相同的溶液中,溶质的物质的量浓度:c(NH3•H2O)>c(CH3COONH4)>c(NH4Cl)>c(NH4HSO4) | |
| B. | 常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Cl-)>c(NH4+)>c(H+)=c(OH-) | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量盐酸大于醋酸 | |
| D. | 将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均减小 |
5.高铁电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应式为3Zn+2K2FeO4+8H2O═3Zn(OH)2+2Fe(OH)3+4KOH.下列叙述正确的是( )
| A. | 放电时,正极区溶液的pH增大 | |
| B. | 放电时,负极反应式为3Zn-6e-=3Zn2+ | |
| C. | 充电时,每转移3 mol电子,阳极有1 mol Fe(OH)3被还原 | |
| D. | 充电时,电池的锌电极接电源的正极 |
2.下列有关说法错误的是( )
| A. | 有机高分子化合物的相对分子质量很大,但其结构是若干链节的重复 | |
| B. | 生成有机高分子化合物的反应只有加聚反应 | |
| C. | 塑料、合成橡胶和合成纤维这三大合成材料,都主要是以石油、煤和天然气为原料生产的 | |
| D. | 聚乙烯塑料的主要成分聚乙烯是由石油裂解产物乙烯通过聚合反应制得的 |
19.下列图象分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法正确的是( )


| A. | 石墨转变为金刚石是吸热反应 | |
| B. | 白磷比红磷稳定 | |
| C. | S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2,则△H1<△H2 | |
| D. | CO(g)+H2O(g)═CO2(g)+H2(g)△H>0 |
3.两种常见的非金属元素A与B,与常见的三种金属元素C、D、E,A的一种单质是自然界硬度最大的物质,B与C的单质在加热条件下反应生成淡黄色化合物X,D的单质既能与盐酸、也能与NaOH溶液反应生成H2.E的单质与水蒸气反应,生成一种黑色固体Y.请回答下列问题:
(1)X与A的稳定氧化物反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2↑.
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因Al熔点低,氧化铝熔点高,所以熔化的铝被氧化铝兜着,并不滴落.
(3)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有BC.
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为2Na+Cu2++2H2O=Cu(OH)2↓+2Na++H2↑.将所得沉淀过滤、洗涤、灼烧,可得到$\frac{40a}{23}$g固体.
(4)为探究黑色固体Y的成分,两探究小组分别用黑色固体Y进行以下实验.
①乙组得到的黑色粉末是FeO.
②甲组步骤1中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O.
③乙组步骤4中,溶液变红的原因为Fe2+被氧化为Fe3+,Fe3++遇SCN-显红色;溶液褪色可能的原因是SCN-被过量Cl2氧化;验证方法为向溶液中再加入KSCN溶液,溶液呈红色,则说明之前SCN-被过量Cl2氧化.
(1)X与A的稳定氧化物反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2↑.
(2)将D的单质用砂纸打磨,然后灼烧,液态的D并不滴落的原因Al熔点低,氧化铝熔点高,所以熔化的铝被氧化铝兜着,并不滴落.
(3)ag C的单质投入足量CuSO4溶液中,下列实验现象正确的有BC.
A.钠沉在溶液底部 B.熔化成银色光亮的小球
C.小球四处游动发出”嘶嘶”的声音 D.生成红色固体物质
可能的离子方程式为2Na+Cu2++2H2O=Cu(OH)2↓+2Na++H2↑.将所得沉淀过滤、洗涤、灼烧,可得到$\frac{40a}{23}$g固体.
(4)为探究黑色固体Y的成分,两探究小组分别用黑色固体Y进行以下实验.
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色固体粉末加入稀盐酸 | 溶解,无气泡 | 溶解,无气泡 |
| 2 | 取步骤1中溶液,滴加酸性KMnO4溶液 | 紫色褪去 | 紫色褪去 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
②甲组步骤1中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O.
③乙组步骤4中,溶液变红的原因为Fe2+被氧化为Fe3+,Fe3++遇SCN-显红色;溶液褪色可能的原因是SCN-被过量Cl2氧化;验证方法为向溶液中再加入KSCN溶液,溶液呈红色,则说明之前SCN-被过量Cl2氧化.
4.下列说法正确的是( )
| A. | 苯和乙烯均含有碳碳双键,均可使溴的CCl4溶液褪色 | |
| B. | 苯( )的一氯代物有一种,丙烷的一氯代物也有一种 )的一氯代物有一种,丙烷的一氯代物也有一种 | |
| C. | 乙醇和乙烯均可与酸性高锰酸钾发生反应 | |
| D. | 所有的有机物都很容易燃烧 |
 .
. 如图的转化关系中,已知A是由短周期元素组成的盐,H与Na2O2可发生化合反应,生成的盐与Ba2+反应可生成不溶于稀G的白色沉淀,一个D分子中含有10个电子.
如图的转化关系中,已知A是由短周期元素组成的盐,H与Na2O2可发生化合反应,生成的盐与Ba2+反应可生成不溶于稀G的白色沉淀,一个D分子中含有10个电子.