题目内容
9.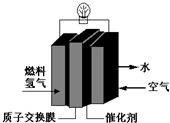 第29届奥运会期间,作为马拉松领跑车和电视拍摄车的汽车,装着“绿色心脏”--质子交换膜燃料电池,其工作原理如图所示.
第29届奥运会期间,作为马拉松领跑车和电视拍摄车的汽车,装着“绿色心脏”--质子交换膜燃料电池,其工作原理如图所示.其电池总反应式为:O2+2H2═2H2O
正极反应为O2+4H++4e-=2H2O,
负极反应为2H2-4e-=4H+.
分析 在燃料电池中,通入燃料的电极是负极,该极上发生失电子的氧化反应,通入氧气的电极是正极,该极上发生得电子的还原反应,总反应即为燃料燃烧的化学方程式.
解答 解:根据燃料电池的电极反应规律:通入空气(含有氧气)的电极是正极,发生还原反应,反应式为 O2+4H++4e-=2H2O;
通入燃料氢气的电极是负极,反应式为2H2-4e-=4H+;
总反应即为燃料燃烧的化学方程式,即O2+2H2═2H2O.
故答案为:2H2+O2═2H2O;O2+4H++4e-=2H2O; 2H2-4e-=4H+.
点评 本题考查学生燃料电池的工作原理知识,注意把握正负极电极方程式的书写等内容,题目难度不大.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
16.标准状况下H2S和O2混合气体100mL,经点燃反应至完全,所得气体干燥后,恢复到原来状况时体积为10mL,该10mL气体可能是( )
| A. | H2S和SO2 | B. | O2和SO2 | C. | H2S或SO2 | D. | 只有SO2 |
20.1828年,填平无机物与有机物间鸿沟的科学巨匠乌勒将一种无机盐直接转变为有机物尿素[CO(NH2)2],乌勒使用的无机盐是( )
| A. | NH4NO3 | B. | (NH4)2CO3 | C. | NH4CNO | D. | CH3COONH4 |
17.下列叙述不正确的是( )
| A. | 焊锡(锡铅合金)熔点比金属锡高 | |
| B. | 生成物的能量与反应物的能量一般都不相等 | |
| C. | 使用催化剂,可加快反应速率,但不能改变反应限度 | |
| D. | 用CaSO4可降低盐碱地(含Na2CO3、NaCl)土壤的碱性 |
18.下列有关化学用语表示正确的是( )
| A. | CO2分子比例模型: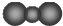 | B. | 硫离子的结构示意图为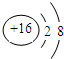 | ||
| C. | NH4Cl的电子式为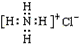 | D. | 中子数为20的氯原子${\;}_{17}^{37}$Cl |