题目内容
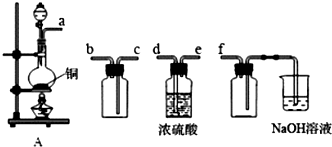
15.0.1mol某烃在20L(标况)过量O2中完全燃烧后,将生成的混合气体与足量的Na2O2反应增重15g,剩余气体为14.4L(标况),则该烃为( )| A. | C2H6 | B. | C3H6 | C. | C4H8 | D. | C5H10 |
分析 氧气过量,由4H~O2~2H2O、C~O2~CO2、2Na2O2+2H2O=4NaOH+O2↑、2Na2O2+2CO2=2Na2CO3+O2可知,反应前后气体减少的体积是CO2体积的一半;Na2O2粉末与1molH2O及1molCO2反应,质量会分别增加2g、28g,根据n=$\frac{V}{{V}_{m}}$计算出生成二氧化碳的物质的量,结合总质量列式计算出水的物质的量,从而可计算出该有机物的分子式.
解答 解:氧气过量,由4H~O2~2H2O、C~O2~CO2、2Na2O2+2H2O=4NaOH+O2↑、2Na2O2+2CO2=2Na2CO3+O2可知,O2减少的体积是CO2体积的一半;Na2O2粉末与1molH2O及1molCO2反应,质量会分别增加2g、28g,
n(CO2)=$\frac{2×(20-14.4)L}{22.4L/mol}$=0.5mol,
28n(CO2)+2n(H2O)=15g,
n(H2O)=0.5mol,
则0.1mol该烃含C原子0.5 mol,含H原子1 mol,则其分子式为:C5H10,
故选D.
点评 本题考查了有机物分子式、结构简式的确定,侧重于学生的分析、计算能力的考查,题目难度中等,根据反应方程式得出二氧化碳的物质的量为解答关键,注意差量法在化学计算中的应用方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列关于乙烯说法正确的是( )
| A. | 乙烯使酸性高锰酸钾溶液及溴的四氯化碳溶液褪色原理相同 | |
| B. | 工业利用乙烯水化法制乙醇,是发生了取代反应 | |
| C. | 乙烯在空气中燃烧,发生明亮并带有淡蓝色的火焰 | |
| D. | 水果运输中为延长果实的成熟期,常在车厢里放置浸泡过高锰酸钾溶液的硅藻土 |
3.某有机物在O2中充分燃烧,生成CO2和H2O的物质的量比为1:1,下列说法正确的是( )
| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:1 | ||
| C. | 该有机物可能为烃 | D. | 此有机物的最简式为CH2 |
10.某溶液可能含有Cl-、SO42-、NH4+、Fe3+、Al3+和K+.取该溶液100mL,加入过量NaOH 溶液,加热,得到0.02mol 气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到 1.6g 固体;向上述滤液中加足量BaCl2溶液,得到 4.66g 不溶于盐酸的沉淀.由此可知原溶液中( )
| A. | 至少存在5 种离子 | |
| B. | SO42-、NH4+、Fe3+、一定存在,Cl-、K+、Al3+可能存在 | |
| C. | K+一定存在,Al3+可能存在 | |
| D. | Cl-一定存在,且c(Cl-)≥0.4mol/L |
20.如表为元素周期表的一部分,根据元素①~⑧在周期表中的位置,按要求回答下列问题.
(1)在元素①~⑧中,金属性最强的元素是Na(填元素符号),最不容易形成化合物的元素是Ar(填元素符号).
(2)用电子式表示⑦的气态氢化物的形成过程 .
.
(3)③、④、⑥中原子半径由大到小的顺序是Na>S>F(填元素符号).
(4)表中两种元素的原子按1:1组成的常见液态化合物X易被催化分解.某同学取5支大小相同的试管,各加入等物质的量浓度等体积的X溶液,分别进行下列实验,研究外界条件对X分解反应速率的影响,实验记录如下表所示.
①第一组实验目的是:相同条件下,探究温度对该反应速率的影响.实验2的催化剂A是FeCl3溶液.
②第二组实验中,实验4的温度t是20,发生反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.第二组实验结论是:在20℃(或相同条件下),MnO2可以加快H2O2分解的反应速率.
| 族 周期 | IA | 0族 | ||||||
| 1 | ① | IIA | IIIA | ⅣA | VA | ⅥA | VIIA | |
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
(2)用电子式表示⑦的气态氢化物的形成过程
 .
.(3)③、④、⑥中原子半径由大到小的顺序是Na>S>F(填元素符号).
(4)表中两种元素的原子按1:1组成的常见液态化合物X易被催化分解.某同学取5支大小相同的试管,各加入等物质的量浓度等体积的X溶液,分别进行下列实验,研究外界条件对X分解反应速率的影响,实验记录如下表所示.
| 序号 | 条件 | 现象 | 结论 | ||
| 温度/℃ | 催化剂 | ||||
| 第一组 | 1 | 40 | FeCl3溶液 | 快速产生大量气泡 | 相同条件下,温度升高,化学反应速率加快 |
| 2 | 20 | A | 缓慢产生适量气泡 | ||
| 3 | 5 | FeCl3溶液 | 缓慢产生极少量气泡 | ||
| 第二组 | 4 | t | MnO2 | 快速产生大量气泡 | |
| 5 | 20 | 无 | 缓慢产生极少量气泡 | ||
②第二组实验中,实验4的温度t是20,发生反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.第二组实验结论是:在20℃(或相同条件下),MnO2可以加快H2O2分解的反应速率.
3. 表是元素周期表的前三周期:
表是元素周期表的前三周期:
回答下列问题:
(1)J元素的元素的名称:氩.
(2)G元素与I 元素形成的化合物的电子式是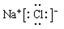 ,A、G、E形成的化合物中含有的化学键类型为离子键、共价键.
,A、G、E形成的化合物中含有的化学键类型为离子键、共价键.
(3)表格中十种元素的最高氧化物对应的水化物中,酸性最强的是HClO4,属于两性氢氧化物的是Al(OH)3(用化合物的化学式表示).
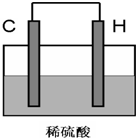
(4)将H单质与C的一种单质(导体)按如图装置连接,其中C极为正极(填正或负),并写出该电极反应式为:2H++2e-=H2↑.
 表是元素周期表的前三周期:
表是元素周期表的前三周期:| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 一 | A | |||||||
| 二 | B | C | D | E | F | |||
| 三 | G | H | I | J |
(1)J元素的元素的名称:氩.
(2)G元素与I 元素形成的化合物的电子式是
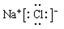 ,A、G、E形成的化合物中含有的化学键类型为离子键、共价键.
,A、G、E形成的化合物中含有的化学键类型为离子键、共价键.(3)表格中十种元素的最高氧化物对应的水化物中,酸性最强的是HClO4,属于两性氢氧化物的是Al(OH)3(用化合物的化学式表示).
(4)将H单质与C的一种单质(导体)按如图装置连接,其中C极为正极(填正或负),并写出该电极反应式为:2H++2e-=H2↑.