题目内容
18.用1.0mol•L-1的NaOH溶液滴定某浓度的硫酸,下列操作会使测定结果偏低的是( )| A. | 滴定开始时,碱式滴定管内有气泡,滴定过程中气泡消失 | |
| B. | 起始计数仰视 | |
| C. | 滴定结束时,还有1滴NaOH溶液挂在尖嘴上 | |
| D. | 用蒸馏水将锥形瓶壁的H2SO4冲下 |
分析 根据c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,若消耗标准液体积偏大,测定结果偏高,相反则偏低,以此判断浓度的误差.
解答 解:A.滴定开始时,碱式滴定管内有气泡,滴定过程中气泡消失,导致消耗标准液体积偏大,测定结果偏高,故A错误;
B.起始计数仰视,导致读出的标准液体积偏小,测定结果偏低,故B正确;
C.滴定结束时,还有1滴NaOH溶液挂在尖嘴上,导致消耗标准液体积偏大,测定结果偏高,故C错误;
D.用蒸馏水将锥形瓶壁的H2SO4冲下,对滴定结果无影响,故D错误;
故选B.
点评 本题考查了中和滴定中的误差分析,题目难度中等,明确中和滴定操作方法为解答关键,注意根据c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$分析滴定误差,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
相关题目
2.化学与人类生产、生活、社会可持续发展密切相关,下列说法正确的是( )
| A. | 凡含有添加剂的食物对人体健康均有害,不宜食用 | |
| B. | 硅胶可用作食品干燥剂 | |
| C. | “天宫一号”使用的碳纤维,是一种新型有机高分子材料 | |
| D. | 工业上燃烧煤时,加入少量石灰石是为了减少CO2的排放 |
13.下列物质能使品红溶液褪色的是( )
①活性炭 ②过氧化钠 ③氯水 ④二氧化硫.
①活性炭 ②过氧化钠 ③氯水 ④二氧化硫.
| A. | ①③④ | B. | ②③④ | C. | ①②④ | D. | ①②③④ |
3. 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是
A.B.( )
 现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是
现有短周期主族元素X、Y、Z、R、T.R原子最外层电子数是电子层数的2倍,Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡.五种元素的原子半径与原子序数的关系如图所示.下列推断正确的是A.B.( )
| A. | 原子半径和离子半径均满足:Y<Z | |
| B. | 氢化物的沸点排序:Y>T>R | |
| C. | 最高价氧化物对应的水化物的酸性:T<R | |
| D. | 单质氧化性:Y>R>T |
10.最外层电子数为4的原子,其荷电核数可能为( )
| A. | 8 | B. | 14 | C. | 7 | D. | 17 |
8.LiOH常用于制备锂离子电池正极材料.工业上常利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法正确的是( )

| A. | a是电源的负极 | |
| B. | B极区电解液为LiOH溶液 | |
| C. | A电极的电极反应式为4OH--4e-=2H2O+O2↑ | |
| D. | 每产生标准状况下2.24L氢气,就有0.1mol阳离子通过交换膜进入阴极区 |
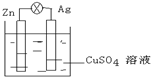 (1)在如图的银锌原电池中,银为正极,电极上发生的是还原反应(“氧化”或“还原”),电极反应式是Cu2++2e-═Cu.锌片上观察到的现象为锌片溶解,电极反应式为Zn-2e-═Zn2+.
(1)在如图的银锌原电池中,银为正极,电极上发生的是还原反应(“氧化”或“还原”),电极反应式是Cu2++2e-═Cu.锌片上观察到的现象为锌片溶解,电极反应式为Zn-2e-═Zn2+.