题目内容
9.有机物A和B的分子中都有2个碳原子,室温时A为气体,B为液体,A在催化剂作用下与水反应生成一种含氧的化合物C,催化氧化C可生成B,B与新制的氢氧化铜共热生成D,C与D一定条件下可发生酯化反应生成E.写出以上各物质的结构简式和相应的化学方程式.分析 有机物A和B的分子中都有2个碳原子,室温时A为气体,B为液体,A在催化剂作用下与水反应生成一种含氧的化合物C,催化氧化C可生成B,B与新制的氢氧化铜共热生成D,C与D一定条件下可发生酯化反应生成E,
CH2=CH2和H2O反应生成CH3CH2OH,CH3CH2OH发生催化氧化反应生成CH3CHO,CH3CHO能和新制氢氧化铜悬浊液反应生成CH3COOH,CH3CH2OH和CH3COOH在一定条件下发生酯化反应生成CH3COOCH2CH3,且CH2=CH2是气体,CH3CH2OH是液体,符合转化关系,所以A、B、C、D、E分别是CH2=CH2、CH3CHO、CH3CH2OH、CH3COOH、CH3COOCH2CH3,据此分析解答.
解答 解:有机物A和B的分子中都有2个碳原子,室温时A为气体,B为液体,A在催化剂作用下与水反应生成一种含氧的化合物C,催化氧化C可生成B,B与新制的氢氧化铜共热生成D,C与D一定条件下可发生酯化反应生成E,CH2=CH2和H2O反应生成CH3CH2OH,CH3CH2OH发生催化氧化反应生成CH3CHO,CH3CHO能和新制氢氧化铜悬浊液反应生成CH3COOH,CH3CH2OH和CH3COOH在一定条件下发生酯化反应生成CH3COOCH2CH3,且CH2=CH2是气体,CH3CH2OH是液体,符合转化关系,所以A、B、C、D、E分别是CH2=CH2、CH3CHO、CH3CH2OH、CH3COOH、CH3COOCH2CH3,
A生成C的反应方程式为CH2=CH2+H2O$\stackrel{一定条件下}{→}$CH3CH2OH;
C发生催化氧化反应生成B,2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O,
C和D发生酯化反应生成E,反应方程式为CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O,
答:A、B、C、D、E及发生的反应分别为:CH2=CH2、CH3CHO、CH3CH2OH、CH3COOH、CH3COOCH2CH3,
CH2=CH2+H2O$\stackrel{一定条件下}{→}$CH3CH2OH;
2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O;
CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
点评 本题考查有机物推断,为高频考点,涉及烯烃、醇、醛、羧酸、酯之间的转化,明确常见有机物官能团及其性质及物质之间的转化是解本题关键,难点是乙醛和新制氢氧化铜悬浊液的反应方程式的书写,题目难度不大.

| A. | 1 mol SO2 (g)的能量总和大于1 mo S(s)和1 mol O2(g)的能量总和 | |
| B. | 加入合适的催化剂,可增加单位质量的硫燃烧放出的热量 | |
| C. | S(g)+O2(g)→SO2(g)+Q1 kJ;Q1的值大于297.23 | |
| D. | 足量的硫粉与标况下1升氧气反应生成1升二氧化硫气体时放出297.23 kJ热量 |
| A. | 氯乙烷和水 | B. | 乙醇与水 | C. | 乙酸乙酯和乙醇 | D. | 漠苯与苯 |
| A. | 酸式滴定管在装酸液前用标准盐酸溶液润洗2~3次 | |
| B. | 开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失 | |
| C. | 锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度 | |
| D. | 盛NaOH溶液的锥形瓶滴定前未用NaOH溶液润洗 |
| 实验步骤 | 实验现象 |
| 1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色. |
| 2.向新制得的Na2S溶液中滴加少量新制的氯水 | B.有气体产生,溶液变成浅红色 |
| 3.将一小块钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| 4.将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| 5.将铝条投入稀盐酸中 | E.生成淡黄色沉淀 |
(1)实验目的:探究同周期主族元素性质递变规律.
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液.仪器:①烧杯,②试管,③胶头滴管,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等.
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
| 实验内容 | 实验现象 | 离子方程式 |
| 1 | ||
| 2 | ||
| 3 | ||
| 4 | ||
| 5 |
(5)实验结论:同周期元素随原子序数增大,元素金属性逐渐减弱,非金属性逐渐增强;
[探究实验二]一定条件下,氯化镁与四氯化钛的混合物可作烯烃聚合反应
的催化剂.为了探究温度、氯化镁固体的含水量以及粉碎方式对该催化剂催化
效果的影响,设计如下对比实验:
| 实验 序号 | 氯化镁固体中氯元素含量/% | 温度/℃ | 粉碎方式/ | 催化效果/g•g-1 |
| 1 | 70.97 | 20 | 滚动球磨 | 3.9×104 |
| 2 | 74.45 | 20 | 滚动球磨 | 5.0×104 |
| 3 | 74.45 | 20 | 振动球磨 | 5.9×104 |
| 4 | ω | 100 | 振动球磨 |
(6)表中ω=74.45;
(7)从实验1、2可以得出的结论是:氯化镁固体含水量越高,催化剂催化效果越差是:..
| A. | 滴定开始时,碱式滴定管内有气泡,滴定过程中气泡消失 | |
| B. | 起始计数仰视 | |
| C. | 滴定结束时,还有1滴NaOH溶液挂在尖嘴上 | |
| D. | 用蒸馏水将锥形瓶壁的H2SO4冲下 |
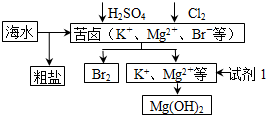
| A. | 工业上,电解熔融MgO冶炼金属镁可减小能耗 | |
| B. | 从苦卤中提取Br2的反应的离子方程式为2Br -+Cl2═2Cl-+Br2 | |
| C. | 试剂1可以选用石灰乳 | |
| D. | 可用BaCl2溶液除去粗盐中的SO42- |



 ;
; ;
;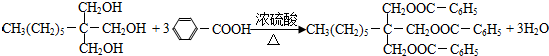 .
.