题目内容
6.下列关于σ键和π键说法正确的是( )| A. | σ键是由两个p电子“肩并肩”重叠形成的 | |
| B. | σ键和π键都是共价键,σ键比π键更稳定 | |
| C. | 乙烯分子中的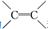 和乙炔分子中的-C≡C-都是π键 和乙炔分子中的-C≡C-都是π键 | |
| D. | H2分子中含有σ键,HCl分子中含π键 |
分析 A.σ键为s或p电子“头碰头”重叠形成;
B.重叠方式大的较稳定;
C.乙烯中双键、乙炔中三键均含一个σ键;
D.H2、HCl中均为σ键.
解答 解:A.σ键是由两个p电子或s电子或s-p电子“头碰头”重叠形成的,故A错误;
B.σ键和π键都是共价键,但σ键重叠方式大,比π键更稳定,故B正确;
C.乙烯中双键、乙炔中三键均含一个σ键,三键中含2个π键,故C错误;
D.H2、HCl中均为共价单键,均为σ键,故D错误;
故选B.
点评 本题考查共价键的类型,为高频考点,把握σ键与π键的形成及常见物质中的化学键为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
1.25℃时,下列溶液中水的电离程度最小的是( )
| A. | pH=2 的CH3COOH溶液 | B. | 0.01 mol/L Na2CO3溶液 | ||
| C. | 0.001 mol/L盐酸 | D. | pH=10氨水 |
14.取一定量的Fe、Cu的混合物粉末,平均分成A、B、C、D、E五等份,分别向每一份中加入一定量的稀硝酸,实验中收集到的NO气体(惟一还原产物)的体积及所得剩余物的质量记录如表(所有体积均在标准状况下测定):
(1)A组实验后17.2g剩余固体为Fe、Cu,B组实验后8g剩余固体为Cu.(均填写化学式)
(2)实验中每次所取混合物中铁的物质的量为0.20mol.
(3)若C组金属恰好反应完,则反应后溶液中的金属阳离子为:Fe2+、Cu2+、Fe3+,物质的量之比是:n(Fe2+):n(Cu2+):n(Fe3+)=6:9:2.
| 实验序号 | A | B | C | D | E |
| 硝酸溶液体积 | 100ml | 200mL | 300mL | 400mL | 500mL |
| 剩余固体的质量 | 17.2g | 8g | 0g | 0g | 0g |
| 气体体积 | 2.24L | 4.48L | 6.72L | 7.84L | 7.84L |
(2)实验中每次所取混合物中铁的物质的量为0.20mol.
(3)若C组金属恰好反应完,则反应后溶液中的金属阳离子为:Fe2+、Cu2+、Fe3+,物质的量之比是:n(Fe2+):n(Cu2+):n(Fe3+)=6:9:2.
11.下列对一些物质或化学反应的分类以及依据正确的是( )
| A. | 豆浆是胶体,因为豆浆中的分散质粒子直径在1nm~100nm之间 | |
| B. | NaCl溶液是电解质,因为NaCl溶液能导电 | |
| C. | Na和H2O的反应不是离子反应,因为反应中没有离子参加 | |
| D. | H2SO4是酸,因为H2SO4中含有氢元素 |
15.一定量的Na、Mg、Al分别与足量的盐酸反应,放出氢气的质量之比为1:2:4,则Na、Mg、Al三种金属的物质的量之比为( )
| A. | 1:1:1 | B. | 4:2:1 | C. | 2:3:4 | D. | 3:3:4 |
16.A、B、C、D、E、F六种化合物,其中A、B、C、D、E均由短周期元素组成,焰色反应均为黄色,B、C、E均由三种元素组成.B、C的组成元素相同,且C的摩尔质量比B大80g/mol,回答:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为AC
A、离子键 B、极性共价键 C、非极性共价键 D、氢键
(2)下表为B与F实验的部分内容
写出B与稀H2SO4反应的离子方程式S2O32-+2H+=S↓+SO2↑+H2O,
写出②中反应方程式FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;
(3)现由6种粒子Mn2+、MnO4-、H+、H2O、X2Y82-(C中含有的阴离子)、XY42-完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4-需氧化剂的物质的量为2.5mol
(4)化合物D和E相互转化D$?_{CO_{2}+H_{2}O}^{△}$ E,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为AC
A、离子键 B、极性共价键 C、非极性共价键 D、氢键
(2)下表为B与F实验的部分内容
| ①在含B的溶液中加入稀H2SO4,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
| ②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色 |
| ③将实验②得到的红褐色液体加热蒸发,灼烧,最终得到红棕色固体 |
写出②中反应方程式FeCl3+3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3HCl;
(3)现由6种粒子Mn2+、MnO4-、H+、H2O、X2Y82-(C中含有的阴离子)、XY42-完成一个离子方程式,已知Mn2+为还原剂,得到1mol MnO4-需氧化剂的物质的量为2.5mol
(4)化合物D和E相互转化D$?_{CO_{2}+H_{2}O}^{△}$ E,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增生2.20g,则E•xH2O的化学式为Na2C03•7H2O.
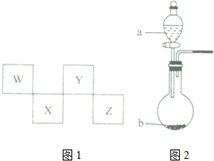 W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.
W、X、Y、Z四种短周期元素在周期表中的位置如图1所示,其中Y与钠元素和氢元素均可形成原子个数1:1和1:2的化合物.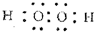 ,Z在周期表中的位置第三周期ⅦA族.
,Z在周期表中的位置第三周期ⅦA族.