题目内容
15.一定量的Na、Mg、Al分别与足量的盐酸反应,放出氢气的质量之比为1:2:4,则Na、Mg、Al三种金属的物质的量之比为( )| A. | 1:1:1 | B. | 4:2:1 | C. | 2:3:4 | D. | 3:3:4 |
分析 酸足量,金属均完全反应,结合电子守恒计算.
解答 解:酸足量,金属完全反应,放出氢气的质量之比为1:2:4,即放出氢气的物质的量比为1:2:4,
设生成氢气分别为1mol、2mol、4mol,
由电子守恒可知,Na、Mg、Al三种金属的物质的量之比为1mol:$\frac{2mol}{(2-0)}$:$\frac{4mol}{(3-0)}$=3:3:4,
故选D.
点评 本题考查氧化还原的计算,为高频考点,把握酸足量及电子守恒为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
10.下列说法错误的是( )
| A. | 镁在空气中燃烧发出耀眼的白光,可用于制作照明弹 | |
| B. | 在一定条件下可实现下列转化MgCl2(溶液)→Mg(OH)2→MgO | |
| C. | 通过置换反应可实现由Mg到MgO的转化 | |
| D. | 镁与稀硝酸反应的离子方程式为:Mg+2H+═Mg+H2↑ |
6.下列关于σ键和π键说法正确的是( )
| A. | σ键是由两个p电子“肩并肩”重叠形成的 | |
| B. | σ键和π键都是共价键,σ键比π键更稳定 | |
| C. | 乙烯分子中的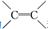 和乙炔分子中的-C≡C-都是π键 和乙炔分子中的-C≡C-都是π键 | |
| D. | H2分子中含有σ键,HCl分子中含π键 |
3.由不同种类的原子组成的物质可能是( )
①纯净物
②混合物
③单质
④化合物
⑤金属
⑥非金属
⑦酸
⑧碱
⑨盐
⑩氧化物.
①纯净物
②混合物
③单质
④化合物
⑤金属
⑥非金属
⑦酸
⑧碱
⑨盐
⑩氧化物.
| A. | ①③⑤⑦⑨ | B. | ②④⑧⑩ | C. | ①③ | D. | 全部 |
10.下列实验基本操作及注意事项中,主要出于安全考虑的是( )
| A. | 实验剩余的药品不能放回原试剂瓶 | |
| B. | 酒精灯内酒精不能多于酒精灯容积的2/3 | |
| C. | 实验结束后将试管清洗干净 | |
| D. | 胶头滴管不能交叉使用 |
4.在2L密闭容器内,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
(1)用O2表示从0~2s内该反应的平均速率v=0.015mol•L-1•S-1.
(2)能说明该反应已经达到平衡状态的是AD
A.容器内压强不变 B.容器内气体的密度保持不变
C.v正(NO)=2v正(O2) D.v正(NO2)=v逆(NO2)
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
(2)能说明该反应已经达到平衡状态的是AD
A.容器内压强不变 B.容器内气体的密度保持不变
C.v正(NO)=2v正(O2) D.v正(NO2)=v逆(NO2)
5.下列有关说法不正确的是( )
| A. | 镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| B. | 手机上用的锂离子电池属于二次电池 | |
| C. | 燃料电池能把化学能转化成电能 | |
| D. | 已知反应2CO(g)=2C(s)+O2(g)的△H>0、△S<0,那么高温下可自发进行 |
 肼(N2H4)的性质类似于氨气,易溶于水,是塑料、橡胶发泡剂的原料.将肼蒸气通入Cu0胶体中,可发生如图所示的转化.
肼(N2H4)的性质类似于氨气,易溶于水,是塑料、橡胶发泡剂的原料.将肼蒸气通入Cu0胶体中,可发生如图所示的转化.