题目内容
1.25℃时,下列溶液中水的电离程度最小的是( )| A. | pH=2 的CH3COOH溶液 | B. | 0.01 mol/L Na2CO3溶液 | ||
| C. | 0.001 mol/L盐酸 | D. | pH=10氨水 |
分析 酸或碱抑制水电离,含有弱离子的盐促进水电离,酸中氢离子浓度越大或碱中氢氧根离子浓度越大,抑制水电离程度越大,据此分析解答.
解答 解:酸或碱抑制水电离,含有弱离子的盐促进水电离,酸中氢离子浓度越大或碱中氢氧根离子浓度越大,抑制水电离程度越大,碳酸钠是强碱弱酸盐,碳酸根离子水解而促进水电离,水的电离程度较大;
醋酸、盐酸是酸而氨水是碱溶液,所以醋酸、盐酸和氨水都抑制水电离,醋酸中氢离子浓度是0.01mol/L、盐酸中氢离子浓度是0.001mol/L、氨水中氢氧根离子浓度为0.0001mol/L,所以水电离程度大小顺序是B>D>C>A,则水电离程度最小的是醋酸,
故选A.
点评 本题以弱电解质的电离及盐类水解为载体考查水的电离,明确影响水电离因素是解本题关键,注意:酸、碱抑制水电离与氢离子或氢氧根离子浓度有关,题目难度不大.

练习册系列答案
相关题目
11.已知某条件下,合成氨反应的数据如下:N2+3H2?NH3
起始浓度/mol•L-1 1.0 3.0 0.2
2s末浓度/mol•L-1 0.6 1.8 1.0
4s末浓度/mol•L-1 0.4 1.2 1.4
当用氨气浓度的增加来表示该反应的速率时,下列说法中正确的是( )
起始浓度/mol•L-1 1.0 3.0 0.2
2s末浓度/mol•L-1 0.6 1.8 1.0
4s末浓度/mol•L-1 0.4 1.2 1.4
当用氨气浓度的增加来表示该反应的速率时,下列说法中正确的是( )
| A. | 2 s末氨气的反应速率=0.4 mol•(L•s)-1 | |
| B. | 前2 s时间内氢气的平均反应速率=0.9 mol•(L•s)-1 | |
| C. | 前4 s时间内氮气的平均反应速率=0.1mol•(L•s)-1 | |
| D. | 2~4 s时间内氨气的平均反应速率=0.2 mol•(L•s)-1 |
16. 把0.1molMnO2粉末加入50ml过氧化氢的溶液里(密度为1.1g•mL-1),在标准状况下,放出气体的体积V和时间t的关系曲线如图所示.a、b、c、d各点反应速率最快的是( )
把0.1molMnO2粉末加入50ml过氧化氢的溶液里(密度为1.1g•mL-1),在标准状况下,放出气体的体积V和时间t的关系曲线如图所示.a、b、c、d各点反应速率最快的是( )
 把0.1molMnO2粉末加入50ml过氧化氢的溶液里(密度为1.1g•mL-1),在标准状况下,放出气体的体积V和时间t的关系曲线如图所示.a、b、c、d各点反应速率最快的是( )
把0.1molMnO2粉末加入50ml过氧化氢的溶液里(密度为1.1g•mL-1),在标准状况下,放出气体的体积V和时间t的关系曲线如图所示.a、b、c、d各点反应速率最快的是( )| A. | a | B. | b | C. | c | D. | d |
6.下列实验操作都能够达到预期目的是( )
①用精密pH试纸测得某溶液pH为3.5
②用米汤直接检验食用盐中是否含有碘元素
③用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
④滴入酚酞溶液确定纯碱中有无烧碱
⑤用酸式滴定管量取20.00mL高锰酸钾酸性溶液
⑥蒸干AlCl3溶液可得纯净的无水氯化铝.
①用精密pH试纸测得某溶液pH为3.5
②用米汤直接检验食用盐中是否含有碘元素
③用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
④滴入酚酞溶液确定纯碱中有无烧碱
⑤用酸式滴定管量取20.00mL高锰酸钾酸性溶液
⑥蒸干AlCl3溶液可得纯净的无水氯化铝.
| A. | ②④⑥ | B. | ②⑥ | C. | ①⑤ | D. | ④⑤⑥ |
10.下列说法错误的是( )
| A. | 镁在空气中燃烧发出耀眼的白光,可用于制作照明弹 | |
| B. | 在一定条件下可实现下列转化MgCl2(溶液)→Mg(OH)2→MgO | |
| C. | 通过置换反应可实现由Mg到MgO的转化 | |
| D. | 镁与稀硝酸反应的离子方程式为:Mg+2H+═Mg+H2↑ |
6.下列关于σ键和π键说法正确的是( )
| A. | σ键是由两个p电子“肩并肩”重叠形成的 | |
| B. | σ键和π键都是共价键,σ键比π键更稳定 | |
| C. | 乙烯分子中的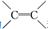 和乙炔分子中的-C≡C-都是π键 和乙炔分子中的-C≡C-都是π键 | |
| D. | H2分子中含有σ键,HCl分子中含π键 |



 .写出A与溴水的反应方程式
.写出A与溴水的反应方程式 +3Br2→
+3Br2→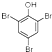 ↓+3HBr
↓+3HBr 或
或 (任写一个).
(任写一个). .
. 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).
