题目内容
6.在标准状况下,气体摩尔体积约为22.4L/mol,则标准状况下1.5molH2的体积约为( )| A. | 44.8L | B. | 5L | C. | 11.2L | D. | 33.6L |
分析 标准状况下Vm=22.4L/mol,根据V=nVm计算.
解答 解:标准状况下的1.5molH2的体积为1.5mol×22.4L/mol=33.6L,
故选D.
点评 本题考查物质的量与气体体积换算,侧重于学生的计算能力的考查,难度不大,注意相关计算公式的运用.

练习册系列答案
相关题目
6.短周期元素A、B、C的原子序数依次增大,其族序数之和为13,且C的族序数是B的族序数的3倍.下列说法正确的是( )
| A. | 三种元素的原子半径:B最小 | |
| B. | 最高价氧化物对应的水化物:仅B呈碱性 | |
| C. | 常温下,B在A、C的最高价氧化物对应的水化物浓溶液中会发生钝化 | |
| D. | A、B、C的氧化物都是形成酸雨的罪魁祸首 |
14.有七种物质:①甲烷、②苯、③聚乙烯、④1,3-戊二烯、⑤2-丁炔、⑥甲苯、⑦环己烯,既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的是( )
| A. | ③④⑤ | B. | ④⑤⑦ | C. | ④⑤ | D. | ③④⑤⑦ |
1.甲烷分子中的四个氢原子都可以被取代.若甲烷分子中的四个氢原子都被苯基取代,则可得到分子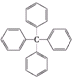 .对该分子的描述正确的是( )
.对该分子的描述正确的是( )
 .对该分子的描述正确的是( )
.对该分子的描述正确的是( )| A. | 分子式为C25H20 | B. | 其不是芳香烃 | ||
| C. | 所有碳原子都在同一平面上 | D. | 该物质为脂环烃 |
18.下列说法不正确的是( )
| A. | 纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应 | |
| B. | 分子式是C3H8O的所有同分异构体共3种 | |
| C. | 用乙醇和浓H2SO4制备乙烯时,不可用水浴加热控制反应的温度 | |
| D. | 迷迭香酸结构如图: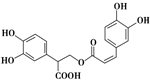 1 mol 迷迭香酸最多能和含6 mol NaOH的水溶液完全反应 1 mol 迷迭香酸最多能和含6 mol NaOH的水溶液完全反应 |
15.下列关于有机物的说法正确的是( )
| A. | 有机物不能通过人工的方法合成 | |
| B. | 烃是指燃烧后只生成CO2和H2O的有机物 | |
| C. | 有机物只含有碳、氢两种元素 | |
| D. | 含碳元素的化合物不一定都属于有机物 |