题目内容
K2FeO4-Zn 碱电池工作时,K2FeO4所在一极的产物为Fe(OH)3,其电极反应为 ;该电池总反应的离子方程式为 .
考点:化学电源新型电池
专题:电化学专题
分析:K2FeO4-Zn也可以组成碱性电池,K2FeO4所在一极的产物为Fe(OH)3,则K2FeO4在电池中作为正极材料,发生还原反应,负极为锌失电子发生氧化反应,以此解答该题.
解答:
解:K2FeO4-Zn也可以组成碱性电池,K2FeO4所在一极的产物为Fe(OH)3,则K2FeO4在电池中作为正极材料,发生还原反应,被还原生成Fe(OH)3,电极方程式为FeO42-+3e-+4H2O=Fe(OH)3+5OH-,负极反应为Zn-2e-+2OH-=Zn(OH)2,总反应为3Zn+2FeO42-+8H2O=3Zn(OH)2+2Fe(OH)3+4OH-,
故答案为:FeO42-+3e-+4H2O=Fe(OH)3+5OH-;3Zn+2FeO42-+8H2O=3Zn(OH)2+2Fe(OH)3+4OH-.
故答案为:FeO42-+3e-+4H2O=Fe(OH)3+5OH-;3Zn+2FeO42-+8H2O=3Zn(OH)2+2Fe(OH)3+4OH-.
点评:本题考查了原电池原理,为高频考点,侧重于学生的分析能力的考查,明确正负极的判断方法、正负极上发生的反应即可解答,难点是电极方程式的书写,为易错点.

练习册系列答案
相关题目
将一定质量和钠投入24.6g水中,形成t°C的NaOH饱和溶液31.2g,t°C时,NaOH的溶解度为( )
| A、48g | B、62.5g |
| C、23g | D、31g |
分别取下列溶液各2毫升,用水稀释到20毫升,溶液的pH 由3.0变成4.0,则该溶液是( )
(a)一元强酸(b)二元弱酸(c)一元弱酸(d)二元强酸.
(a)一元强酸(b)二元弱酸(c)一元弱酸(d)二元强酸.
| A、(a) | B、(b) |
| C、(a)(c) | D、(a)(d) |
在解释下列物质性质的变化规律与物质结构间的因果关系时,与化学键的强弱无关的变化规律是( )
| A、HF、HCl、HBr、HI的热稳定依次减弱 |
| B、金刚石的硬度大于硅,其熔、沸点也高于硅 |
| C、NaF、NaCl、NaBr、NaI的熔点依次减小 |
| D、F2、Cl2、Br2、I2的熔、沸点逐渐升高 |
下列化学用语或模型正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、甲烷分子的比例模型: |
C、羟基的电子式: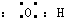 |
| D、葡萄糖的最简式:C6H12O6 |
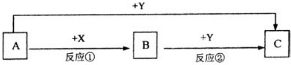 A、B、C三种物质的转化关系如图所示(部分产物已略去)
A、B、C三种物质的转化关系如图所示(部分产物已略去)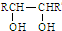
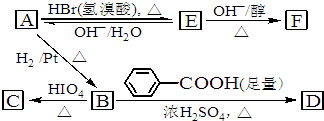
 氢是一种重要的非金属元素.氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用.
氢是一种重要的非金属元素.氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用.