题目内容
将锌片和铜片用导线连接置于稀硫酸溶液中,下列叙述错误的是( )
| A、锌片做负极,锌发生还原反应 |
| B、铜片做正极 |
| C、溶液中的pH值增大 |
| D、溶液中的H+向正极移动 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:锌比铜活泼,锌为负极,被氧化,发生Zn-2e-═Zn2+,铜为正极,发生还原反应,电极方程式为2H++2e-═H2↑,溶液中阳离子向正极移动,以此解答该题.
解答:
解:A.锌比铜活泼,锌为负极,被氧化,发生氧化反应,故A错误;
B.锌比铜活泼,锌为负极,铜为正极,故B正确;
C.电池的总反应为:Zn+2H+═H2↑+Zn2+,反应消耗氢离子,则溶液中的pH值增大,故C正确;
D.溶液中阳离子向正极移动,溶液中的H+向正极移动,故D正确.
故选:A.
B.锌比铜活泼,锌为负极,铜为正极,故B正确;
C.电池的总反应为:Zn+2H+═H2↑+Zn2+,反应消耗氢离子,则溶液中的pH值增大,故C正确;
D.溶液中阳离子向正极移动,溶液中的H+向正极移动,故D正确.
故选:A.
点评:本题综合考查了原电池知识,侧重于学生的分析能力的考查,注意把握原电池反应原理和两极变化,明确原电池放电时电极方程式的书写是解本题的关键,难度不大.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
如图装置中,通电后观察到Cu极溶解.下列说法中错误的是( )
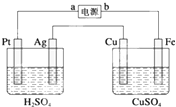

| A、a极是直流电源的正极 | ||
| B、Fe极是阳极 | ||
C、Pt极产生的气体体积是Ag极产生气体体积为
| ||
| D、硫酸铜溶液的浓度不变 |
101kPa时辛烷的燃烧热为5518kJ?mol-1,强酸与强碱在稀溶液中发生反应时的中和热为57.3kJ?mol-1,则下列热化学方程式书写正确的是( )
A、C8H18(1)+
| ||||
B、C8H18(1)+
| ||||
| C、H+(aq)+OH-(aq)═H2O(aq);△H=一57.3 kJ?mol-1 | ||||
D、NaOH(aq)+
|
下列变化中,一定要加入氧化剂才能实现的是( )
| A、HCl→H2 |
| B、Cl2→NaClO |
| C、CO→CO2 |
| D、FeCl3→FeCl2 |
下列有关化学用语表示正确的是( )
| A、乙烯的结构简式:C2H4 | ||
B、中子数为146、质子数为92的铀(U)原子
| ||
C、氯原子的结构示意图: | ||
D、氢氧根离子的电子式: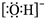 |