题目内容
下列现象或反应的原理解释正确的是( )
| 现象或反应 | 原理解释 | |
| A | 锌与盐酸反应时,加入几滴氯化铜溶液可加快反应速率 | 氯化铜作反应的催化剂 |
| B | 将一小块金属钠投入水中,金属钠熔成小球 | 该反应△H>0 |
| C | 镀层破损后,镀锡铁比镀锌铁易腐蚀 | 锡比锌活泼 |
| D | 常温下,测得0.1mol/L醋酸溶液的pH=4 | 醋酸是弱电解质 |
| A、A | B、B | C、C | D、D |
考点:化学反应速率的影响因素,金属的电化学腐蚀与防护,弱电解质在水溶液中的电离平衡,钠的化学性质
专题:基本概念与基本理论
分析:A.锌置换出铜,形成原电池反应;
B.金属钠熔成小球,说明反应放热;
C.镀层破损后,镀锡铁中铁为负极,易被氧化;
D.0.1mol/L醋酸溶液的pH=4,说明醋酸部分电离.
B.金属钠熔成小球,说明反应放热;
C.镀层破损后,镀锡铁中铁为负极,易被氧化;
D.0.1mol/L醋酸溶液的pH=4,说明醋酸部分电离.
解答:
解:A.锌置换出铜,形成原电池反应,反应速率增大,故A错误;
B.金属钠熔成小球,说明反应放热,该反应△H<0,故B错误;
C.镀层破损后,镀锡铁中铁为负极,易被氧化,铁比锡活泼,故C错误;
D.0.1mol/L醋酸溶液的pH=4,说明醋酸部分电离,故D正确.
故选D.
B.金属钠熔成小球,说明反应放热,该反应△H<0,故B错误;
C.镀层破损后,镀锡铁中铁为负极,易被氧化,铁比锡活泼,故C错误;
D.0.1mol/L醋酸溶液的pH=4,说明醋酸部分电离,故D正确.
故选D.
点评:本题考查较为综合,涉及多方面的知识,为高频常见题型,注意把握原电池以及金属的腐蚀,钠与水反应的特点以及弱电解质的电离特点,难度不大.

练习册系列答案
相关题目
下列物质的分离提纯主要是利用化学性质的是( )
| A、沙里淘金 |
| B、利用磁铁分离铁屑和沙混合物 |
| C、利用自来水制备蒸馏水 |
| D、粗盐提纯中除去粗盐含有的可溶性杂质 |
 下表各组物质中,满足如图物质(或其水溶液)一步转化关系的选项是( )
下表各组物质中,满足如图物质(或其水溶液)一步转化关系的选项是( )| 选项 | X | Y | Z |
| A | Na | NaOH | Na2O |
| B | Cu | CuSO4 | Cu(OH)2 |
| C | Cl2 | FeCl2 | FeCl3 |
| D | CO2 | Na2CO3 | NaHCO3 |
| A、A | B、B | C、C | D、D |
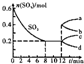 在一个2L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的变化如图所示.下列判断正确的是( )
在一个2L的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的变化如图所示.下列判断正确的是( )| A、用O2表示0~8 min内该反应的平均速率为0.025 mol?(L?min)-1 |
| B、升高温度,达到新平衡时的化学平衡常数比原平衡的小 |
| C、容器内压强保持不变时反应处于平衡状态 |
| D、第12min时,容器压强到1L,则SO3的变化曲线为a |
将锌片和铜片用导线连接置于稀硫酸溶液中,下列叙述错误的是( )
| A、锌片做负极,锌发生还原反应 |
| B、铜片做正极 |
| C、溶液中的pH值增大 |
| D、溶液中的H+向正极移动 |
下列有关物质的保存方法,不正确的是( )
| A、液氯储存在钢瓶中 |
| B、浓硫酸储存在铝制容器中 |
| C、金属钠保存在煤油中 |
| D、氢氧化钠溶液保存在带玻璃塞的玻璃试剂瓶中 |
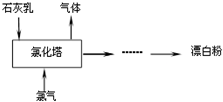 氯气是重要的化工原料.
氯气是重要的化工原料.