题目内容
【题目】设NA为阿佛加德罗常数,下列说法不正确的是( )
A.标准状况下,22.4 L氦气中含2NA个氦原子
B.18g水中含有的电子数为10NA
C.1mol Cl2与金属Na完全反应,可以得到2NA个电子
D.在1L2mol/L的硝酸镁溶液中含有的硝酸根离子数为4NA
【答案】A
【解析】
A.标准状况下,22.4 L氦气的物质的量为![]() =1mol,氦气为单原子分子,故含有氦原子数为NA,故A符合题意;
=1mol,氦气为单原子分子,故含有氦原子数为NA,故A符合题意;
B.18g水的物质的量为![]() =1mol,1个H2O分子中含有电子数为(8+2×1)=10个,因此1mol水中含有的电子数为10NA,故B不符合题意;
=1mol,1个H2O分子中含有电子数为(8+2×1)=10个,因此1mol水中含有的电子数为10NA,故B不符合题意;
C.Cl2与金属Na完全反应,氯元素化合价从0价降低为-1价,因此1mol Cl2完全反应得到电子2mol,其数目为2NA,故C不符合题意;
D.硝酸镁化学式为Mg(NO3)2,1L2mol/L的硝酸镁溶液中含有硝酸镁的物质的量为1L×2mol/L=2mol,硝酸根离子数为4NA,故D不符合题意;
故答案为:A。

【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 |
|
| HClO |
|
|
电离平衡常数 |
|
|
|
|
|
(1)25℃时,等浓度的![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液,3种溶液的pH由大到小的顺序为________。
溶液,3种溶液的pH由大到小的顺序为________。
(2)工业上可用氨水除去尾气![]() 。将
。将![]() 通入氨水中,当
通入氨水中,当![]() 降至
降至![]() _____。
_____。
(3)常温下,用![]() 溶液滴定
溶液滴定![]() 溶液所得滴定曲线如图:
溶液所得滴定曲线如图:
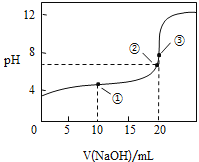
①在整个实验过程中,不需要的仪器或用品是 ______(填序号).
![]() 容量瓶 b 锥形瓶c 滴定管夹d 漏斗e 玻璃棒f 滴定管
容量瓶 b 锥形瓶c 滴定管夹d 漏斗e 玻璃棒f 滴定管
②到达滴定终点的标志是 _____________ .
③下列操作会导致测定结果偏高的是 ______ .
A 碱式滴定管在装液前未用标准NaOH溶液润洗
B 滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C 碱式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D 达到滴定终点时,仰视读数
④如图点①所示溶液中![]() __________
__________![]() 填“>”“<”或“=”,下同,点②所示溶液中:
填“>”“<”或“=”,下同,点②所示溶液中:![]() ________
________![]() ,点③所示溶液中所有离子浓度由大到小的顺序为:_________。
,点③所示溶液中所有离子浓度由大到小的顺序为:_________。