题目内容
16.常温下,在10mL0.1mol•L-1Na2CO3溶液中逐滴加入0.1mol•L-1HCl溶液,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数变化如图所示(CO2因逸出未画出,忽略因气体逸出引起的溶液体积变化),下列说法正确的是( )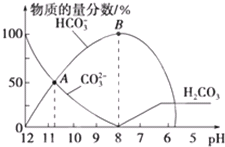
| A. | 当溶液的pH=7时,溶液的总体积为20mL(若忽略溶液混合后体积的变化) | |
| B. | 在0.1mol/L 的Na2CO3溶液中:c(Na+)+c(H+)═c(CO32-)+c(OH-)+c(HCO3-) | |
| C. | 在A点所示的溶液中:c(CO32-)═c(HCO3-)>c(H+)>c(OH-) | |
| D. | 在B点所示的溶液中,浓度最大的阳离子是Na+ |
分析 A.当溶液总体积为20mL时,加入的HCl体积是10mL,二者恰好完全反应生成NaHCO3,NaHCO3是强碱弱酸酸式盐,HCO3-水解程度大于其电离程度,溶液呈碱性;
B.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断;
C.根据图知,A点溶液中c(CO32-)═c(HCO3-),溶液的pH>7,溶液呈碱性;
D.B点溶液中溶质为NaHCO3,钠离子不水解,HCO3-水解但程度较小.
解答 解:A.当溶液总体积为20mL时,加入的HCl体积是10mL,二者恰好完全反应生成NaHCO3,NaHCO3是强碱弱酸酸式盐,HCO3-水解程度大于其电离程度,溶液呈碱性,根据图知,pH=7时溶液中的溶质为碳酸氢钠和NaCl,加入的盐酸体积大于10mL,故A错误;
B.任何电解质溶液中都存在电荷守恒,根据电荷守恒得:c(Na+)+c(H+)═2c(CO32-)+c(OH-)+c(HCO3-),故B错误;
C.根据图知,A点溶液中c(CO32-)═c(HCO3-),溶液的pH>7,溶液呈碱性,所以c(H+)<c(OH-),故C错误;
D.B点溶液中溶质为NaHCO3,钠离子不水解,HCO3-水解但程度较小,所以溶液中浓度最大的阳离子是Na+,故D正确;
故选D.
点评 本题考查离子浓度大小比较,为高频考点,侧重考查学生分析判断及识图能力,明确各点溶液中溶质成分及其性质是解本题关键,注意:碳酸钠溶液中滴加稀盐酸时,碳酸钠先生成NaHCO3,然后NaHCO3再和稀盐酸反应,为易错点.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
7.根据题给信息,完成下列各小题:
Ⅰ、某造纸厂排出的废水,经取样分析其中除了含有游离汞、纤维素以及其它的有机物外,其它成分为c(Na+)=4×10-4mol/L,c(SO42-)=2.5×10-4mol/L,c(Cl-)=1.6×10-5 mol/L,c(NO3-)=1.4×10-5 mol/L,c(Ca2+)=1.5×10-5 mol/L,则该废水的pH为4.
Ⅱ、有四种一元酸HA、HB、HC、HD,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大;NaA溶液呈中性;1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质的量浓度的HB、HC分别作导电性试验,发现后者的导电性比前者强,则这四种酸的酸性由强到弱的顺序为HA>HC>HB>HD.
Ⅲ、常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得
溶液的pH如下表:
请回答:
(1)从①组情况分析,HA是强酸还是弱酸弱酸(填“强酸”或“弱酸”);
(2)①组实验所得混合溶液中由水电离出的c(OH-)=10-5mol•L-1.
(3)②组情况表明,c大于0.2mol/L(选填“大于”、“小于”或“等于”).混合液中离子浓度c(A-)与c(Na+)的大小关系是c(A-)=c(Na+).
(4)从③组实验结果分析,说明HA的电离程度大于NaA的水解程度(选填“大于”、“小于”或“等于”),该混合溶液中离子浓度由大到小的顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
Ⅰ、某造纸厂排出的废水,经取样分析其中除了含有游离汞、纤维素以及其它的有机物外,其它成分为c(Na+)=4×10-4mol/L,c(SO42-)=2.5×10-4mol/L,c(Cl-)=1.6×10-5 mol/L,c(NO3-)=1.4×10-5 mol/L,c(Ca2+)=1.5×10-5 mol/L,则该废水的pH为4.
Ⅱ、有四种一元酸HA、HB、HC、HD,相同物质的量浓度的NaD和NaB溶液的pH,前者比后者大;NaA溶液呈中性;1mol/L的KC溶液遇酚酞试液呈红色;同体积、同物质的量浓度的HB、HC分别作导电性试验,发现后者的导电性比前者强,则这四种酸的酸性由强到弱的顺序为HA>HC>HB>HD.
Ⅲ、常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得
溶液的pH如下表:
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(1)从①组情况分析,HA是强酸还是弱酸弱酸(填“强酸”或“弱酸”);
(2)①组实验所得混合溶液中由水电离出的c(OH-)=10-5mol•L-1.
(3)②组情况表明,c大于0.2mol/L(选填“大于”、“小于”或“等于”).混合液中离子浓度c(A-)与c(Na+)的大小关系是c(A-)=c(Na+).
(4)从③组实验结果分析,说明HA的电离程度大于NaA的水解程度(选填“大于”、“小于”或“等于”),该混合溶液中离子浓度由大到小的顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
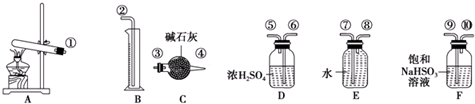
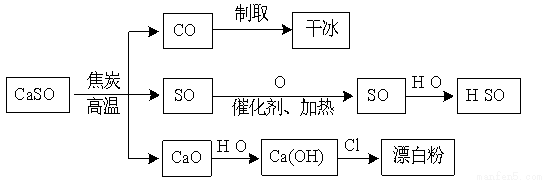
1.硫酸铜受热分解生成氧化铜和气体,加热温度不同,气体成分也不同.气体成分可能含SO2、SO3和O2中的一种、两种或三种.某化学课外活动小组通过设计探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式.实验用到的仪器如图所示:
【提出猜想】
Ⅰ.所得气体的成分可能只含SO3一种;
Ⅱ.所得气体的成分可能含有SO2、O2两种;
Ⅲ.所得气体的成分可能含有SO3、SO2、O2三种.
【实验探究】
实验操作过程略.
已知实验结束时,硫酸铜完全分解.
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口的连接顺序为:①→⑨→⑩→⑥→⑤→③→④→⑧→⑦→②(填接口序号).
(2)若实验结束时B中量筒没有收集到水,则证明猜想Ⅰ正确.
(3)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同,数据如下:
请通过计算,推断出第一小组和第二小组的实验条件下CuSO4分解的化学方程式.
第一小组:2CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+2SO2↑+O2↑;
第二小组:4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO2↑+2SO3↑+O2↑.

【提出猜想】
Ⅰ.所得气体的成分可能只含SO3一种;
Ⅱ.所得气体的成分可能含有SO2、O2两种;
Ⅲ.所得气体的成分可能含有SO3、SO2、O2三种.
【实验探究】
实验操作过程略.
已知实验结束时,硫酸铜完全分解.
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口的连接顺序为:①→⑨→⑩→⑥→⑤→③→④→⑧→⑦→②(填接口序号).
(2)若实验结束时B中量筒没有收集到水,则证明猜想Ⅰ正确.
(3)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同,数据如下:
| 实验小组 | 称取CuSO4的质量/g | 装置C增加的质量/g | 量筒中水的体积折算成标准状况下气体的体积/mL |
| 一 | 6.4 | 2.56 | 448 |
| 二 | 6.4 | 2.56 | 224 |
第一小组:2CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+2SO2↑+O2↑;
第二小组:4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO2↑+2SO3↑+O2↑.
8.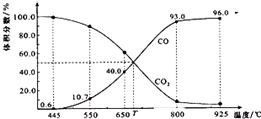 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(p分)=气体总压(p总)×体积分数.下列说法正确的是( )
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(p分)=气体总压(p总)×体积分数.下列说法正确的是( )
 一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(p分)=气体总压(p总)×体积分数.下列说法正确的是( )
一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)?2CO(g).平衡时,体系中气体体积分数与温度的关系如图所示:已知:气体分压(p分)=气体总压(p总)×体积分数.下列说法正确的是( )| A. | 550℃时,若充入惰性气体,v正、v逆 均减小,平衡不移动 | |
| B. | 650℃时,反应达平衡后CO2的转化率为25.0% | |
| C. | T℃时,若充入等体积的CO2和CO,平衡不移动 | |
| D. | 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=24.p总 |
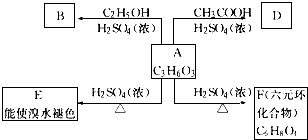
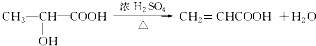 ;A→F
;A→F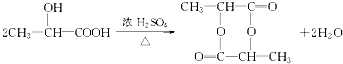
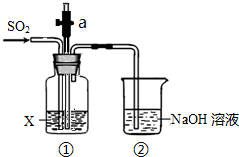 某实验小组用如图所示装置探究SO2的性质.
某实验小组用如图所示装置探究SO2的性质.