题目内容
16.阿伏伽德罗常数的值约为6.02×1023mol-1,下列叙述中不正确的是( )①12.4g白磷晶体中含有的P-P键数约是0.6×6.02×1023
②0.5mol•L-1 Mg(NO3)2溶液中含有NO3-的数目为1×6.02×1023
③7.8g Na2S和Na2O2的混合物中含有的阴离子数大于0.1×6.02×1023
④2mol SO2和1mol O2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2×6.02×1023
⑤0.1mol Fe与0.1mol氯气反应时失去的电子数为0.3×6.02×1023
⑥含0.2mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1×6.02×1023.
| A. | ①④⑥ | B. | ①③④⑤⑥ | C. | ②③⑤⑥ | D. | ③④⑤⑥ |
分析 ①求出白磷的物质的量,然后根据1mol白磷中含6molP-P键来分析;
②溶液体积不明确;
③Na2S和Na2O2的摩尔质量均为78g/mol,且两者中均含2个钠离子和1个阴离子;
④SO2和O2的反应是可逆反应,不能进行彻底;
⑤0.1mol Fe与0.1mol氯气反应时铁过量,根据氯气的量来分析转移的电子数;
⑥铜只能与浓硫酸反应,与稀硫酸不反应.
解答 解:①12.4g白磷的物质的量为0.1mol,而1mol白磷中含6molP-P键,故0.1mol白磷中含0.6molp-p键即0.6NA个,故正确;
②溶液体积不明确,故溶液中的硝酸根的个数无法计算,故错误;
③Na2S和Na2O2的摩尔质量均为78g/mol,故7.8g混合物的物质的量为0.1mol,且两者中均含2个钠离子和1个阴离子,故0.1mol混合物中含由0.1mol阴离子即0.1NA个,故错误;
④SO2和O2的反应是可逆反应,不能向右进行彻底,故反应后分子个数大于2NA个,故正确;
⑤0.1mol Fe与0.1mol氯气反应时铁过量,根据氯气的量来分析转移的电子数,由于氯气反应后变为-1价,故0.1mol氯气转移0.2mol电子即0.2NA个,故错误;
⑥铜只能与浓硫酸反应,与稀硫酸不反应,即浓硫酸不能反应完全,则生成的二氧化硫分子个数小于0.1NA个,故错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
7.有关氯的叙述正确的是( )
| A. | 液氯和氯水是同一物质 | |
| B. | 红磷在氯气中燃烧产生红色烟雾 | |
| C. | 氯气与水的反应中氯是氧化剂,水是还原剂 | |
| D. | 用氯制漂白粉是为了得到易贮存的漂白剂 |
4.要使含有Ag+、Mg2+、Ba2+等溶液中的离子逐一形成沉淀析出,下列所选择的试剂及加入试剂的顺序正确的是( )
| A. | H2SO4→HCl→NaOH→CO2 | B. | Na2SO4→NaCl→NH3•H2O | ||
| C. | NaCl→Na2SO4→NaOH | D. | Na2SO4→NaCl→NaOH |
1.电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示.下列说法正确的是( )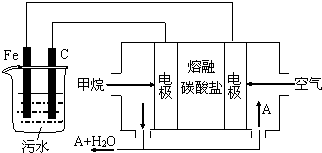

| A. | 该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,则负极的电极反应是CH4+4CO32--8e-═5CO2+2H2O | |
| B. | 实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣,此时,可以向污水中加入适量的稀H2SO4 | |
| C. | 实验过程中,若阴极产生2mol气体,则燃料电池消耗11.2L CH4 | |
| D. | 为了使该电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A参加循环,则A物质是CO32- |
8.电解水﹙H2O﹚和重水﹙D2O﹚的混合物,通电一定时间后,两极共生成气体18.5克,体积为33,6L﹙标况﹚,所生成的气体中重氢﹙D﹚和普氢﹙H﹚的原子个数比是( )
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 1:4 |
5.中学化学中很多“规律”都有其使用范围,下列根据有关“规律”推出的结论合理的是( )
| A. | 根据氧化还原反应的规律,推出强氧化剂遇到强还原剂一定会发生氧化还原反应 | |
| B. | 根据化学反应的规律,推出氢氧化铁可通过化合反应得到 | |
| C. | 根据元素的非金属性较强,其单质也越活泼规律,推出磷单质比N2稳定得多 | |
| D. | 根据CO2通入Ba(NO3)2溶液中无沉淀的规律推测,SO2入Ba(NO3)2溶液中也无沉淀产生 |