题目内容
2.在一定温度下将1mol CO和1mol水蒸气放入一固定容积的密闭容器中,反应CO(g)+H2O(g)?CO2(g)+H2(g)达平衡后,得到0.6mol CO2;再通入0.3mol水蒸气,达到新平衡状态后,CO2的物质的量可能是( )
| A. | 0.9 mol | B. | 0.8 mol | C. | 0.7 mol | D. | 0.6 mol |
分析 反应CO+H2O(g)?CO2+H2达平衡后,加入水蒸气,化学平衡会向着正反应方向进行,但是反应物不可能全部转化为生成物,据此判断.
解答 解:根据题意,利用三段式分析
CO+H2O(g)?CO2 +H2,
初始物质的量:1 1 0 0
变化物质的量:0.6 0.6 0.6 0.6
平衡物质的量:0.4 0.4 0.6 0.6
此时二氧化碳的物质的量是0.6mol,再通入0.3mol水蒸气,化学平衡会向着正反应方向进行,假设一氧化碳全部转化完毕,则会生成二氧化碳和氢气各0.3mol,此时CO2的物质的量0.9mol,但是一氧化碳不会全部转化,所以达到新的平衡后,CO2的物质的量介于0.6mol-0.9mol之间,故选BC.
点评 本题考查了化学平衡的计算分析判断,极值方法的计算应用,题目难度中等.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
10.将下列各组物质溶于水后,得到无色溶液的一组是( )
| A. | K2SO4、HNO3、BaCl2 | B. | NaOH、NH4Cl、Mg(NO3)2 | ||
| C. | NH4HCO3、KCl、NaCl | D. | KMnO4、NaCl、H2SO4 |
17.下列过程属于熵增加的是( )
| A. | 一定条件下水由气态变为液态 | B. | 水总是由高处流向低处 | ||
| C. | 碳酸氢铵在常温情况下分解 | D. | CO点燃时生成CO2 |
7.下列指定反应的离子方程式正确的是( )
| A. | 实验室用烧碱溶液除去尾气中的Cl2:Cl2+OH-═Cl-+HClO | |
| B. | 稀硝酸中加入过量铁粉:Fe+4H++NO3-=Fe3++NO↑+2H2O | |
| C. | 石灰水中加入过量小苏打溶液:2HCO3-+Ca2++2OH-=CaCO3↓+CO32+2H2O | |
| D. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O→2Al(OH)3↓+CO32- |
14.A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如表:A的气态氢化物能使湿润的红色石蕊试纸变蓝;C单质在实验室一般保存在煤油中;F的最高价氧化物对应水化物既能和酸反应又能和强碱反应,G单质是日常生活中用量最大的金属,易被腐蚀.请回答下列问题: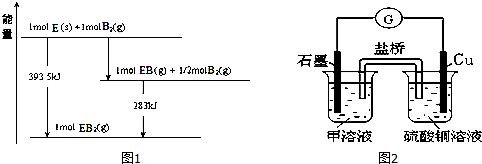
(1)A元素在周期表中的位置是第二周期第VA族.
(2)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中可能引起的环境问题有:(任写一种)酸雨或光化学烟雾;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若使所得溶液pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2 (g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.某同学假设正极产物是Fe2+,请你设计实验证明该假设滴加酸性高锰酸钾溶液,若溶液紫色褪去(或滴加铁氰化钾溶液,产生蓝色沉淀),则产品中含有Fe2+.

| … | E | A | B | ||
| C | … | D |
(2)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中可能引起的环境问题有:(任写一种)酸雨或光化学烟雾;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若使所得溶液pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2 (g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.某同学假设正极产物是Fe2+,请你设计实验证明该假设滴加酸性高锰酸钾溶液,若溶液紫色褪去(或滴加铁氰化钾溶液,产生蓝色沉淀),则产品中含有Fe2+.
12.下列事实中,不能用平衡移动原理解释的是( )
| A. | 开启啤酒瓶后,瓶中马上泛起大量泡沫 | |
| B. | 对CO(g)+NO2(g)═CO2(g)+NO(g)平衡体系增大压强可使其颜色变深 | |
| C. | 常温下,将1mLpH=3的醋酸溶液加水稀释到100mL,测得其pH<5 | |
| D. | 实验室中常用排饱和食盐水的方法收集氯气 |
 氧化铁可溶于稀盐酸.某同学想知道是稀盐酸中的哪种粒子(H2O、H+、Cl-)能使氧化铁溶解.设计如下实验:
氧化铁可溶于稀盐酸.某同学想知道是稀盐酸中的哪种粒子(H2O、H+、Cl-)能使氧化铁溶解.设计如下实验: