题目内容
7.下列指定反应的离子方程式正确的是( )| A. | 实验室用烧碱溶液除去尾气中的Cl2:Cl2+OH-═Cl-+HClO | |
| B. | 稀硝酸中加入过量铁粉:Fe+4H++NO3-=Fe3++NO↑+2H2O | |
| C. | 石灰水中加入过量小苏打溶液:2HCO3-+Ca2++2OH-=CaCO3↓+CO32+2H2O | |
| D. | 向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O→2Al(OH)3↓+CO32- |
分析 A.二者反应生成氯化钠、次氯酸钠和水;
B.过量铁粉和稀硝酸反应生成硝酸亚铁;
C.二者反应生成碳酸钙、碳酸钠和水;
D.二者反应生成氢氧化铝沉淀和碳酸氢钠.
解答 解:A.二者反应生成氯化钠、次氯酸钠和水,离子方程式为Cl2+2OH-═Cl-+H2O+ClO-,故A错误;
B.过量铁粉和稀硝酸反应生成硝酸亚铁,离子方程式为3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故B错误;
C.二者反应生成碳酸钙、碳酸钠和水,离子方程式为2HCO3-+Ca2++2OH-=CaCO3↓+CO32+2H2O,故C正确;
D.二者反应生成氢氧化铝沉淀和碳酸氢钠,离子方程式为AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-,故D错误;
故选C.
点评 本题考查离子方程式正误判断,为高频考点,明确离子方程式书写规则、物质性质是解本题关键,有些化学反应还与反应物的量有关,如BC,D选项的离子方程式还用于制备氢氧化铝.

练习册系列答案
相关题目
17.若有2.8g铁完全被锈蚀掉,则O2得到的电子数(NA为阿伏加德罗常数)是( )
| A. | 0.05NA | B. | 0.1NA | ||
| C. | 0.15NA | D. | 条件不足,不能计算 |
18.下列各组含氯元素的物质中,氯元素化合价相同的一组是( )
| A. | Cl2 HCl | B. | ClO2 NaClO2 | C. | NaCl HClO | D. | KClO3 Ca(ClO3)2 |
2.在一定温度下将1mol CO和1mol水蒸气放入一固定容积的密闭容器中,反应CO(g)+H2O(g)?CO2(g)+H2(g)达平衡后,得到0.6mol CO2;再通入0.3mol水蒸气,达到新平衡状态后,CO2的物质的量可能是
( )
( )
| A. | 0.9 mol | B. | 0.8 mol | C. | 0.7 mol | D. | 0.6 mol |
12.常温下,下列说法正确的是( )
| A. | 0.1 mol/L的NaHA溶液pH=5,则溶液:c(HA-)>c(H+)>c(A2-)>c(H2A) | |
| B. | 等体积、等物质的量浓度的NaCl(aq) 微粒种类大于NaClO(aq)中微粒种类 | |
| C. | pH=3的硫酸溶液中水的电离程度大于pH=11的氨水溶液中水的电离程度 | |
| D. | 体积相同的0.1 mol/L氨水和0.1 mol/L NaOH溶液中和盐酸的能力后者大 |
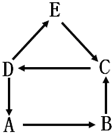 A、B、C、D、E为初中化学常见物质,A是单质,其余为化合物.E可用于检验气体B,它们之间有如图所示的转化关系(“→”表示生成,部分反应物、生成物、反应条件已省略).回答下列问题:
A、B、C、D、E为初中化学常见物质,A是单质,其余为化合物.E可用于检验气体B,它们之间有如图所示的转化关系(“→”表示生成,部分反应物、生成物、反应条件已省略).回答下列问题: