题目内容
下列气态氢化物最稳定的是( )
| A、氟化氢 | B、氯化氢 |
| C、硫化氢 | D、磷化氢 |
考点:非金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:元素的非金属性越强,对应的氢化物越稳定,四种氢化物对应的元素在同一主族,根据元素的非金属性的递变规律判断.
解答:
解:四种氢化物对应的元素在同一主族,同主族元素从上到下元素的非金属性逐渐减弱,则有非金属性F>Cl>Br>I,
元素的非金属性越强,对应的氢化物越稳定,所以氢化物最稳定的是HF,
故选A.
元素的非金属性越强,对应的氢化物越稳定,所以氢化物最稳定的是HF,
故选A.
点评:本题考查元素周期律的递变,题目难度不大,本题注意非金属性与氢化物稳定性之间的关系.

练习册系列答案
相关题目
下列有关说法正确的是( )
| A、所有反应都可以用四种基本反应类型进行概括 |
| B、氧化还原反应可能是复分解反应 |
| C、氧化还原反应可能是化合反应,也可能是分解反应 |
| D、置换反应可能不是氧化还原反应 |
在55℃时,下列说法正确的是( )
| A、向水中加入少量硫酸氢钠固体,促进了水的电离,c(H+)增大,Kw不变 |
| B、pH=3的盐酸和pH=11的氨水等体积混合,溶液显碱性 |
| C、0.1mol/L的(NH4)2SO4溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| D、pH=8的NaHCO3溶液中:c(OH-)=1×10-6mol/L |
能够说明H2(g)+I2(g)?2HI(g)(HI为无色气体)已达平衡状态的是( )
| A、一个H-H键断裂的同时有两个H-I键形成 |
| B、v (H2)正=v (HI)逆时的状态 |
| C、恒温恒容时,反应混合物总质量保持不变的状态 |
| D、恒温恒容时,体系的颜色不再发生变化的状态 |
针铁矿(式量为89)组成元素是Fe、O和H,下列判断错误的是( )
| A、完全溶解89g针铁矿,需要1.0mol/L的稀盐酸至少2L |
| B、针铁矿的化学式是FeO(OH) |
| C、针铁矿中铁元素为+3价 |
| D、44.5g针铁矿约含有6.02×1023个O原子 |
下列物质①甲烷 ②乙烯 ③苯 ④聚乙烯 ⑤乙醇 ⑥环己烷⑦邻二甲苯 ⑧环己烯.其中因反应既能使酸性高锰酸钾溶液退色又能使溴水褪色的是( )
| A、②⑤⑦ | B、③⑦⑧ |
| C、②⑧ | D、②④⑤⑧ |
在一定温度下,在恒定容积的密闭容器中进行的可逆反应A2(g)+B2(g)?2AB(g)达到化学平衡的标志是( )
| A、容器内的总压强不随时间而变化 | ||
B、反应速率V(A2)=V(B2)=
| ||
| C、单位时间内有n molA2生成的同时就有2n molAB生成 | ||
| D、容器内混合气体的密度不随时间而变化 |
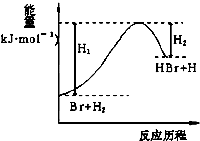 参照反应Br+H2→HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )
参照反应Br+H2→HBr+H的能量对反应历程的示意图,下列叙述中正确的是( )| A、正反应为放热反应 |
| B、断键吸收的总能量大于成键放出的总能量 |
| C、反应物总能量高于生成物总能量 |
| D、升高温度可增大正反应速率,降低逆反应速率 |
有关化学用语正确的是( )
| A、乙烯的最简式C2H4 |
| B、乙醛的结构简式C2H4O |
C、四氯化碳的电子式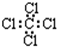 |
| D、乙酸乙酯的分子式C4H8O2 |