题目内容
在55℃时,下列说法正确的是( )
| A、向水中加入少量硫酸氢钠固体,促进了水的电离,c(H+)增大,Kw不变 |
| B、pH=3的盐酸和pH=11的氨水等体积混合,溶液显碱性 |
| C、0.1mol/L的(NH4)2SO4溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) |
| D、pH=8的NaHCO3溶液中:c(OH-)=1×10-6mol/L |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:55℃时,水的离子积常数大于1×10-14,
A.酸或碱抑制水电离,离子积常数只与温度有关;
B.pH=3的盐酸和pH=11的氨水溶液,醋酸浓度小于氨水,二者等体积混合氨水有剩余;
C.硫酸铵是强酸弱碱盐,其溶液呈酸性,再结合电荷守恒判断;
D.pH=8的NaHCO3溶液中c(OH-)>1×10-6mol/L.
A.酸或碱抑制水电离,离子积常数只与温度有关;
B.pH=3的盐酸和pH=11的氨水溶液,醋酸浓度小于氨水,二者等体积混合氨水有剩余;
C.硫酸铵是强酸弱碱盐,其溶液呈酸性,再结合电荷守恒判断;
D.pH=8的NaHCO3溶液中c(OH-)>1×10-6mol/L.
解答:
解:55℃时,水的离子积常数大于1×10-14,
A.硫酸氢钠溶液呈强酸性,所以抑制水电离,加入硫酸氢钠后,硫酸氢钠完全电离,导致溶液中氢离子浓度增大,温度不变,水的离子积常数不变,故A错误;
B.pH=3的盐酸和pH=11的氨水溶液,醋酸浓度小于氨水,二者等体积混合氨水有剩余,所以溶液呈碱性,故B正确;
C.硫酸铵是强酸弱碱盐,其溶液呈酸性则c(H+)>c(OH-)根据电荷守恒得c(NH4+)+c(H+)=c(OH-)+2c(SO42-),所以c(NH4+)>c(SO42-),铵根离子水解程度较小,所以c(SO42-)>c(H+),则溶液中离子浓度大小顺序是c(NH4+)>c(SO42-)>c(H+)>c(OH-),故C正确;
D.55℃时,水的离子积常数大于1×10-14,所以pH=8的NaHCO3溶液中c(OH-)>1×10-6mol/L,故D错误;
故选BC.
A.硫酸氢钠溶液呈强酸性,所以抑制水电离,加入硫酸氢钠后,硫酸氢钠完全电离,导致溶液中氢离子浓度增大,温度不变,水的离子积常数不变,故A错误;
B.pH=3的盐酸和pH=11的氨水溶液,醋酸浓度小于氨水,二者等体积混合氨水有剩余,所以溶液呈碱性,故B正确;
C.硫酸铵是强酸弱碱盐,其溶液呈酸性则c(H+)>c(OH-)根据电荷守恒得c(NH4+)+c(H+)=c(OH-)+2c(SO42-),所以c(NH4+)>c(SO42-),铵根离子水解程度较小,所以c(SO42-)>c(H+),则溶液中离子浓度大小顺序是c(NH4+)>c(SO42-)>c(H+)>c(OH-),故C正确;
D.55℃时,水的离子积常数大于1×10-14,所以pH=8的NaHCO3溶液中c(OH-)>1×10-6mol/L,故D错误;
故选BC.
点评:本题考查了离子浓度大小比较,根据溶液中的溶质及其性质来确定溶液酸碱性,再结合电荷守恒来分析解答,注意该温度不是常温,为易错点.

练习册系列答案
相关题目
下列对化学反应速率(υ)说法正确的是( )
| A、随着反应物浓度增大,活化分子百分数增加,υ增大 |
| B、催化剂降低活化能,使活化分子百分数增加,υ增大 |
| C、在使用酶催化剂时,大幅度提高反应温度可更好地提高υ |
| D、只要反应中有固体、液体物质,压强的变化对υ的影响可以忽略不计 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、使紫色石蕊变红色的溶液:Mg2+、K+、SO42-、NO3- |
| B、使酚酞变红色的溶液:Na+、Cu2+、HCO3-、NO3- |
| C、0.1 mol?L-1AgNO3 溶液:H+、K+、SO42-、Cl- |
| D、加入铝片产生大量H2的溶液:Mg2+、K+、SO42-、Cl- |
同周期的X、Y、Z三种元素,已知它们的最高价氧化物的水化物酸性HXO4>H2YO4>H3ZO4,则下列判断正确的是( )
| A、原子半径:X>Y>Z |
| B、还原性:X->Y2->Z3- |
| C、非金属性:X>Y>Z |
| D、稳定性:ZH3>H2Y>HX |
下列物质能用来干燥CO2气体的是( )
| A、浓H2SO4 |
| B、碱石灰 |
| C、氧化钙 |
| D、氢氧化钠 |
化学是一门实用性强的自然科学,在社会、生产、生活中起着重要的作用,下列说法正确的是( )
| A、金属钠具有强还原性,可用与TiCl4溶液反应制取金属Ti |
B、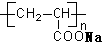 表示一种吸水性高分子树脂 表示一种吸水性高分子树脂 |
| C、用于现代建筑的钢筋混凝土不属于复合材料 |
| D、山东东营广饶县一男子收到网购物品后,因吸入氟乙酸甲酯中毒身亡,氟乙酸甲酯的结构简式为FCH2COOCH3,能与H2发生加成反应,也能被LiAlH4还原 |
现有由等质量的NaHCO3和KHCO3组成的混合物ag,与100mL盐酸反应.关于计算说法不正确的是( )
A、如碳酸氢盐与盐酸恰好完全反应,则盐酸中HCl的物质的量为
| ||||
B、如果盐酸过量,生成的CO2在标准状况下的体积为
| ||||
| C、如果反应后碳酸氢盐有剩余,要计算生成CO2的体积,并不需知道其他条件 | ||||
D、若NaHCO3和KHCO3不是以等质量混合,则a g固体混合物与足量的盐酸完全反应时生成CO2的体积V(CO2)范围是范围是
|
下列气态氢化物最稳定的是( )
| A、氟化氢 | B、氯化氢 |
| C、硫化氢 | D、磷化氢 |
常温时,溶液中下列各组离子一定能够大量共存的是( )
| A、Na+、OH-、AlO2-、S2- |
| B、K+、H+、Br-、HCO3- |
| C、Ba2+、Al3+、Cl-、SiO32- |
| D、K+、Fe3+、NO3-、SO42- |