题目内容
14.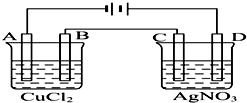 如图为以惰性电极进行电解的装置:
如图为以惰性电极进行电解的装置:(1)写出A、B、C、D各电极上的电极反应式和总反应方程式:
A:Cu2++2e-═Cu,B:2Cl--2e-═Cl2↑,总反应方程式:CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑;
C:2Ag++2e-═2Ag,D:4OH--4e-═2H2O+O2↑,总反应方程式:4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+4HNO3+O2↑.
(2)在A、B、C、D各电极上析出生成物的物质的量之比为2:2:4:1.
(3)A极发生还原反应,B极发生氧化反应.(填“氧化”或是“还原”)
分析 (1)该装置中AC是阴极、BD是阳极,A电极上铜离子放电生成Cu、B电极上氯离子放电生成氯气,所以相当于电解氯化铜生成Cu和氯气;
C电极上银离子放电生成Ag,D电极上氢氧根离子放电生成氧气和水,所以该电池中相当于电解硝酸银和水生成Ag、硝酸和氧气;
(2)A、B、C、D电极反应式分别为Cu2++2e-═Cu、2Cl--2e-═Cl2↑、2Ag++2e-═2Ag、4OH--4e-═2H2O+O2↑,当都转移2mol电子时,A、B、C、D电极上生成的物质物质的量分别是1mol、1mol、2mol、0.5mol;
(3)A电极上得电子发生还原反应,B电极上失电子发生氧化反应.
解答 解:(1)该装置中AC是阴极、BD是阳极,A电极上铜离子放电生成Cu、B电极上氯离子放电生成氯气,所以相当于电解氯化铜生成Cu和氯气,所以A、B、电池反应式分别为Cu2++2e-═Cu、2Cl--2e-═Cl2↑、CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑;
C电极上银离子放电生成Ag,D电极上氢氧根离子放电生成氧气和水,所以该电池中相当于电解硝酸银和水生成Ag、硝酸和氧气,所以C、D、电池反应式分别为2Ag++2e-═2Ag、4OH--4e-═2H2O+O2↑、4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+4HNO3+O2↑;
故答案为:Cu2++2e-═Cu;2Cl--2e-═Cl2↑;CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑;2Ag++2e-═2Ag;4OH--4e-═2H2O+O2↑;4AgNO3+2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+4HNO3+O2↑;
(2)A、B、C、D电极反应式分别为Cu2++2e-═Cu、2Cl--2e-═Cl2↑、2Ag++2e-═2Ag、4OH--4e-═2H2O+O2↑,当都转移2mol电子时,A、B、C、D电极上生成的物质物质的量分别是1mol、1mol、2mol、0.5mol,其物质的量之比=1mol:1mol:2mol:0.5mol=2:2:4:1,
故答案为:2:2:4:1;
(3)A电极上得电子发生还原反应,被还原,B电极上失电子发生氧化反应,被氧化,
故答案为:还原;氧化.
点评 本题考查电解原理,为高频考点,明确离子放电顺序是解本题关键,侧重考查学生分析计算能力,注意:串联电路中各个电极上转移电子守恒,题目难度不大.

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案| A. | 114号元素在周期表中第七周期第VIA族,属于金属元素 | |
| B. | 晶体硅熔点高硬度大,可用于制作光导纤维 | |
| C. | 光束通过下列分散系①云,雾 ②墨水③稀豆浆时,均产生丁达尔效应 | |
| D. | 棉,麻,羊毛及合成纤维完全燃烧都只生成CO2和H2O |
| A. | x=0.5,a=8 | B. | x=0.5,a=10 | C. | x=1.5,a=8 | D. | x=1.5,a=10 |
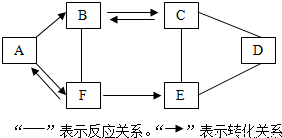
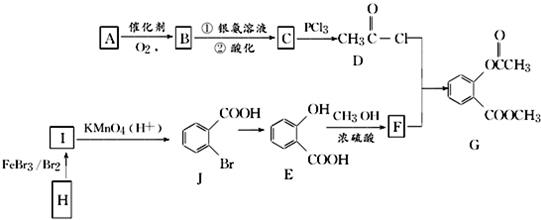
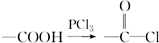
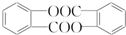 .
.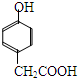 .
.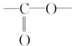 结构
结构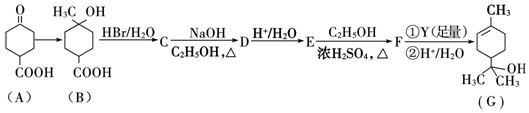
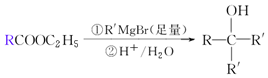
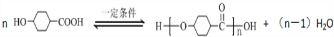 .
. .①核磁共振氢谱有2个吸收峰 ②能发生银镜反应
.①核磁共振氢谱有2个吸收峰 ②能发生银镜反应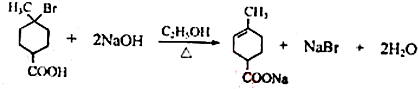 .
.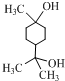 .
.