题目内容
16.某主族元素在周期表中的位置,取决于元素原子的( )| A. | 相对原子质量 | B. | 电子层数和核内中子数 | ||
| C. | 电子层数和最外层电子数 | D. | 金属性和非金属性的强弱 |
分析 对应主族元素,周期数=原子核外电子层数、主族族序数=原子最外层电子数.
解答 解:对应主族元素,周期数=原子核外电子层数、主族族序数=原子最外层电子数,故主族元素在周期表中的位置,取决于元素原子的电子层数和最外层电子数,而相对原子质量、核内中子数、金属性和非金属性的强弱不能确定元素具体位置,故选:C.
点评 本题考查结构与位置关系,比较基础,有利于基础知识的巩固.

练习册系列答案
相关题目
6.下列说法中正确的是( )
| A. | PM 2.5、二氧化碳都属于空气质量日报的内容 | |
| B. | 向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量 | |
| C. | 对“地沟油”进行分馏可得到汽油;玻璃、水泥和陶瓷都属于传统硅酸盐材料 | |
| D. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化台物有关 |
7.下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A. | 将NaHCO3固体加入新制氯水,有无色气泡(H) | |
| B. | 使红色布条褪色(HCl) | |
| C. | 向氯水中加入CuSO4,变蓝色,(H2O) | |
| D. | 滴加AgNO3溶液生成白色沉淀(Cl) |
4.下列反应中,属于氧化还原反应,但不属于四种基本反应类型的是( )
| A. | CaO+H2O═Ca(OH)2 | |
| B. | Zn+2HCl═ZnCl2+H2↑ | |
| C. | NaCl+AgNO3═AgCl+NaNO3 | |
| D. | 2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑ |
1.下列各组离子可能大量共存的是( )
| A. | 常温下水电离出的c(H+)•c(OH-)=10-20的溶液中:Na+、Cl-、S2-、SO32- | |
| B. | 无色溶液中:K+、CH3COO-、HCO3-、MnO4- | |
| C. | 不能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、ClO-、AlO2- | |
| D. | 中性透明溶液:K+、Cl-、NO3-、Fe3+、SO42- |
8.下列物质中,既能与盐酸反应,又能和氢氧化钠溶液反应的是( )
①Al ②Al(OH)3 ③Al2O3 ④AlCl3 ⑤NaAlO2 ⑥NaHCO3.
①Al ②Al(OH)3 ③Al2O3 ④AlCl3 ⑤NaAlO2 ⑥NaHCO3.
| A. | 只有①②③ | B. | 只有①②③⑤⑥ | C. | 只有①②③⑥ | D. | ①②③④⑤⑥ |
5.下列各种情况下一定能大量共存的离子组为( )
| A. | pH=7的溶液中,Fe3+、Cl-、Na+、NO3- | |
| B. | 水电离出的[H+]=1×10-3mol/L 的溶液中Na+、CO32-、Cl-、K+ | |
| C. | pH=1的溶液中NH4+、Cl-、Mg2+、SO42-、 | |
| D. | Al3+、HCO3-、I-、Ca2+ |
 .一定量的该气体燃烧过程的能量变化如图1所示,从图中可以读出E1>E2(填“>”或“<”),该反应放出 (填“放出”或“吸收”)能量.
.一定量的该气体燃烧过程的能量变化如图1所示,从图中可以读出E1>E2(填“>”或“<”),该反应放出 (填“放出”或“吸收”)能量.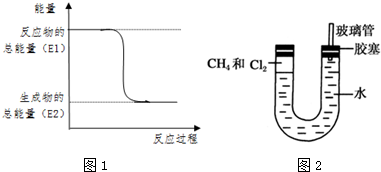
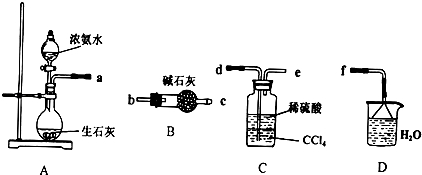 浅绿色的硫酸亚铁铵晶体[又名莫尔盐(NH4)2SO4•FeSO4•6H2O]比绿矾(FeSO4•7H2O)更稳定,常用于定量分析.莫尔盐的一种实验室制法如下:
浅绿色的硫酸亚铁铵晶体[又名莫尔盐(NH4)2SO4•FeSO4•6H2O]比绿矾(FeSO4•7H2O)更稳定,常用于定量分析.莫尔盐的一种实验室制法如下: