题目内容
下列各组物质熔点高低的比较,正确的是( )
| A、晶体硅>金刚石>碳化硅 |
| B、MgO>KCl>NaCl |
| C、Al>Mg>Na |
| D、Cl2>Br2>I2 |
考点:晶体的类型与物质熔点、硬度、导电性等的关系,晶格能的应用
专题:化学键与晶体结构
分析:A.原子晶体中半径越小,共价键越强,熔点越大;
B.离子晶体中阴阳离子半径和越小,电荷越大,熔点越大;
C.金属晶体中原子半径越小,电荷越大,熔点越大;
D.Cl2、Br2、I2 都是分子晶体,分子晶体中相对分子质量越大,熔点越大.
B.离子晶体中阴阳离子半径和越小,电荷越大,熔点越大;
C.金属晶体中原子半径越小,电荷越大,熔点越大;
D.Cl2、Br2、I2 都是分子晶体,分子晶体中相对分子质量越大,熔点越大.
解答:
解:A.晶体硅、金刚石、碳化硅都是原子晶体,因键长C-C<C-Si<Si-Si原子晶体中半径越小,共价键越强,熔点越大,则熔点为金刚石>碳化硅>晶体硅,故A错误;
B.MgO、NaCl、KCl都是离子晶体,阴阳离子半径和大小顺序:MgO<NaCl<KCl,离子晶体中阴阳离子半径和越小,电荷越大,熔点越大;所以熔点高低顺序为:MgO>NaCl>KCl,故B错误;
C.Al、Mg、Na都是金属晶体,Al、Mg、Na电荷数顺序:Al>Mg>Na;原子半径顺序:Al<Mg<Na,金属晶体中原子半径越小,电荷越大,熔点越大,所以熔点顺序:Al>Mg>Na,故C正确;
D.Cl2、Br2、I2都是分子晶体,相对分子质量Cl2<Br2<I2,分子晶体中相对分子质量越大,熔点越大,所以熔点顺序为:Cl2<Br2<I2,故D错误;
故选C.
B.MgO、NaCl、KCl都是离子晶体,阴阳离子半径和大小顺序:MgO<NaCl<KCl,离子晶体中阴阳离子半径和越小,电荷越大,熔点越大;所以熔点高低顺序为:MgO>NaCl>KCl,故B错误;
C.Al、Mg、Na都是金属晶体,Al、Mg、Na电荷数顺序:Al>Mg>Na;原子半径顺序:Al<Mg<Na,金属晶体中原子半径越小,电荷越大,熔点越大,所以熔点顺序:Al>Mg>Na,故C正确;
D.Cl2、Br2、I2都是分子晶体,相对分子质量Cl2<Br2<I2,分子晶体中相对分子质量越大,熔点越大,所以熔点顺序为:Cl2<Br2<I2,故D错误;
故选C.
点评:本题考查晶体熔点的比较,明确不同类型晶体熔点的比较方法是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
在Na2CO3溶液中存在的下列关系不正确的是( )
| A、c(Na+)=2c(CO32-)+2c(H CO3-)+2c(H2 CO3) |
| B、c(Na+)+c(H+)=c(OH-)+c(H CO3-)+c(CO32-) |
| C、c(OH-)=c(H+)+c(H CO3-)+2c(H2 CO3) |
| D、c(Na+)>c(CO32-)>c(OH-)>c(H CO3-) |
下列物质:①盐酸 ②NaOH ③AlCl3 ④明矾 ⑤硫酸铝 ⑥碱式氯化铝 ⑦生石灰.能在水处理中作混凝剂的是( )
| A、①④⑤⑥ | B、②③④⑤ |
| C、③④⑤⑥ | D、全部 |
下列食品添加剂与类别对应正确的一组是( )
| A、着色剂_______苯甲酸钠 |
| B、调味剂_______亚硝酸钠 |
| C、营养强化剂_______酱油中加铁 |
| D、防腐剂_______苋菜红 |
 最近报道说肯德基的新奥尔良烤翅中发现有苏丹红一号,中国国家质量监督检验检疫总局要求清查在国内销售的食品,特别是进口食品,防止含有苏丹红一号的食品在市场中销售使用.苏丹红(1号)结构式如图:下列说法不正确的是( )
最近报道说肯德基的新奥尔良烤翅中发现有苏丹红一号,中国国家质量监督检验检疫总局要求清查在国内销售的食品,特别是进口食品,防止含有苏丹红一号的食品在市场中销售使用.苏丹红(1号)结构式如图:下列说法不正确的是( )| A、苏丹红(1号)的化学式为C16H14N2O |
| B、苏丹红(1号)是芳香族化合物 |
| C、苏丹红(1号)遇FeCl3溶液呈紫色 |
| D、苏丹红(1号)不宜添加食品中用于增色,对人体潜在危害 |
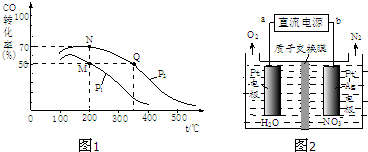
 (1)金属铝是一种常见的金属,铝-海水-空气电池在航海中得到广泛的应用,写出该电池的正极反应方程式:
(1)金属铝是一种常见的金属,铝-海水-空气电池在航海中得到广泛的应用,写出该电池的正极反应方程式: