题目内容
配制一定物质的量浓度的NaOH溶液时,造成实验结果偏低的是( )
①定容时观察液面仰视 ②定容时观察液面俯视③溶解所用的烧杯未洗涤 ④容量瓶中原来有少量蒸馏水.
①定容时观察液面仰视 ②定容时观察液面俯视③溶解所用的烧杯未洗涤 ④容量瓶中原来有少量蒸馏水.
| A、①② | B、②③ | C、①③ | D、③④ |
考点:配制一定物质的量浓度的溶液
专题:物质的量浓度和溶解度专题
分析:根据c=
进行误差分析,如果溶质的物质的量偏小或溶液的体积偏大都使配制溶液浓度偏低,据此分析解答.
| n |
| V |
解答:
解:①定容时观察液面仰视,会导致溶液体积偏大,则造成所配溶液浓度偏低,故①选;
②定容时观察液面俯视,会导致溶液体积偏小,则造成所配溶液浓度偏高,故②不选;
③溶解所用的烧杯未洗涤,会导致溶质NaOH的损失,则造成所配溶液浓度偏低,故③选;
④只要最后溶液的凹液面的最低处与刻度线相切即可,至于水是容量瓶中事先有的,还是后来在配制过程中加入的,对所配溶液的浓度无影响,故④不选.
故选C.
②定容时观察液面俯视,会导致溶液体积偏小,则造成所配溶液浓度偏高,故②不选;
③溶解所用的烧杯未洗涤,会导致溶质NaOH的损失,则造成所配溶液浓度偏低,故③选;
④只要最后溶液的凹液面的最低处与刻度线相切即可,至于水是容量瓶中事先有的,还是后来在配制过程中加入的,对所配溶液的浓度无影响,故④不选.
故选C.
点评:本题考查了误差分析,根据c=
中溶质的物质的量、溶液的体积来分析解答即可,易错选项是D,很多同学认为“容量瓶中原来有少量蒸馏水”对溶液浓度有影响,为易错点.
| n |
| V |

练习册系列答案
相关题目
20g某合金放入足量的稀盐酸中,产生标况下11.2L的氢气,则该合金可能是下列中的( )
| A、Al、Fe合金 |
| B、Mg、Ca合金 |
| C、Na、K合金 |
| D、Mg、Cu合金 |
在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
| A、S(s)+O2(g)=SO2 (g);△H1 S(g)+O2(g)=SO2 (g);△H2 | ||||
| B、2H2(g)+O2 (g)=2H2O(g);△H1 2H2 (g)+O2 (g)=2H2O(l);△H2 | ||||
| C、CO(g)+1/2 O2(g)=CO2(g);△H1 2CO(g)+O2(g)=2CO2(g);△H2 | ||||
D、H2 (g)+Cl2(g)=2HCl(g);△H1
|
25℃时,下列溶液中水的电离程度最大的是( )
| A、0.01 mol/L盐酸 |
| B、0.01 mol/L Na2CO3溶液 |
| C、pH=4 的NaHSO3溶液 |
| D、pH=11氨水 |
下列有关化学用语的说法中不正确的是( )
| A、乙炔的最简式:CH |
| B、乙烯的结构简式:CH2CH2 |
| C、原硅酸的化学式:H4SiO4 |
D、苯的比例模型为: |
关于可逆反应:aA(g)+bB(g)?cC(g)+dD(g)△H的有关图象如下:则下列不正确的是( )
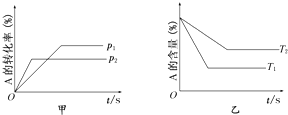

| A、p1<p2 T1>T2 |
| B、减小压强,正逆反应速率都减小,平衡右移 |
| C、△H>0△S>0 |
| D、升高温度,混合气体的平均摩尔质量增大 |
将BaO2放入密闭真空容器中,反应2BaO2(s)?2BaO(s)+O2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是( )
| A、平衡常数减小 |
| B、BaO量不变 |
| C、氧气压强减小 |
| D、BaO2量增加 |
绚丽的焰火将上海世博会开幕式推向了高潮.焰火与高中化学中“焰色反应”知识有关.下列有关“焰色反应”说法中正确的是( )
| A、焰色反应为化学变化 |
| B、所有金属及其化合物灼烧时火焰均有颜色 |
| C、NaCl与Na2CO3灼烧时火焰颜色相同 |
| D、焰色反应均应透过蓝色钴玻璃观察 |