题目内容
关于可逆反应:aA(g)+bB(g)?cC(g)+dD(g)△H的有关图象如下:则下列不正确的是( )
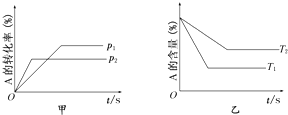

| A、p1<p2 T1>T2 |
| B、减小压强,正逆反应速率都减小,平衡右移 |
| C、△H>0△S>0 |
| D、升高温度,混合气体的平均摩尔质量增大 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:根据“先拐先平数值大”知,P1<P2,T1>T2,增大压强,A的转化率减小,平衡向逆反应方向移动,则该反应是一个反应前后气体体积增大的反应,升高温度,A的含量减小,平衡向正反应方向移动,则正反应是吸热反应.
解答:
解:A、根据“先拐先平数值大”知,P1<P2,T1>T2,故A正确;
B、减小压强,A的转化率增大,平衡向正反应方向移动,正逆反应速率都减小,故B正确;
C、升高温度,A的含量减小,平衡向正反应方向移动,则正反应是吸热反应,△H>0,该反应是一个反应前后气体体积增大的反应,△S>0,故C正确;
D、升高温度,A的含量减小,平衡向正反应方向移动,混合气体的平均摩尔质量=
,反应是一个反应前后气体体积增大的反应,所以分母增大,分子不变,所以混合气体的平均摩尔质量减小,故D错误.
故选D.
B、减小压强,A的转化率增大,平衡向正反应方向移动,正逆反应速率都减小,故B正确;
C、升高温度,A的含量减小,平衡向正反应方向移动,则正反应是吸热反应,△H>0,该反应是一个反应前后气体体积增大的反应,△S>0,故C正确;
D、升高温度,A的含量减小,平衡向正反应方向移动,混合气体的平均摩尔质量=
| 气体总质量 |
| 气体总物质的量 |
故选D.
点评:本题考查了温度、压强对可逆反应平衡的影响,明确“先拐先平数值大”是解本题关键,难度不大.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案
相关题目
下列物质:①水泥 ②玻璃 ③陶瓷 ④水晶,其中属于硅酸盐工业产品的是( )
| A、只有①② | B、只有②④ |
| C、只有①②③ | D、全部 |
在硫酸铝、硫酸钾和明矾的混合溶液中,如果c(SO42-=0.2mol/L,当加等体积的0.2mol/L的KOH溶液时,生成的沉淀恰好溶解,则原混合物中K+的浓度是( )
| A、0.2 mol/L |
| B、0.25 mol/L |
| C、0.45 mol/L |
| D、0.225 mol/L |
一定条件下,在2L密闭容器中进行如下反应:N2+3H2?2NH3,测得2min内N2的物质的量由6mol减少到2mol,则2min内用N2浓度变化表示的该反应的平均反应速率为( )
| A、1 mol/(L?min) |
| B、2mol/(L?min) |
| C、4 mol/(L?min) |
| D、8mol/(L?min) |