题目内容
通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.键能的大小可用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.
通过计算写出反应A2(g)+B2(g)=2AB(g)的热化学方程式.(写出△H的计算过程) .
| 化学键 | A-A | B-B | A-B |
| 生成1mol化学键时放出的能量 | 436kJ?mol-1 | 243kJ?mol-1 | 431kJ?mol-1 |
考点:热化学方程式
专题:化学反应中的能量变化
分析:根据所给的反应和表格中的键能,先判断出断键吸收的热量和成键放出的热量,然后用断键吸收的热量减去成键放出的热量既得反应热.
解答:
解:反应A2(g)+B2(g)=2AB(g)中,旧键断裂吸收的能量为:436kJ?mol-1+243 kJ?mol-1=678kJ?mol-1,新键生成释放的能量为:2×431kJ?mol-1=862kJ?mol-1,△H=678 kJ?mol-1-862kJ?mol-1=-183 kJ?mol-1,
故答案为:反应A2(g)+B2(g)=2AB(g)中,旧键断裂吸收的能量为:436kJ?mol-1+243 kJ?mol-1=678kJ?mol-1,新键生成释放的能量为:2×431kJ?mol-1=862kJ?mol-1,△H=678 kJ?mol-1-862kJ?mol-1=-183 kJ?mol-1,A2(g)+B2(g)=2AB(g)△H=-183 kJ?mol-1.
故答案为:反应A2(g)+B2(g)=2AB(g)中,旧键断裂吸收的能量为:436kJ?mol-1+243 kJ?mol-1=678kJ?mol-1,新键生成释放的能量为:2×431kJ?mol-1=862kJ?mol-1,△H=678 kJ?mol-1-862kJ?mol-1=-183 kJ?mol-1,A2(g)+B2(g)=2AB(g)△H=-183 kJ?mol-1.
点评:本题从断键和成键的角度考查了热化学方程式的书写,难度适中.做题时应注意热化学方程式书写的注意事项,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

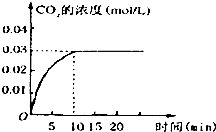 在容积为1L的密闭容器内,加入0.1molCO和0.1molH2O,在催化剂存在的条件下高温加热使其反应.测得CO2的浓度随时间变化的图象如图:
在容积为1L的密闭容器内,加入0.1molCO和0.1molH2O,在催化剂存在的条件下高温加热使其反应.测得CO2的浓度随时间变化的图象如图:
 麻黄素又称黄碱,是我国特定的中药材麻黄中所含的一种生物碱.经我国科学工作者研究发现其结构如图:
麻黄素又称黄碱,是我国特定的中药材麻黄中所含的一种生物碱.经我国科学工作者研究发现其结构如图: