题目内容
 “套管实验”是将一支较小的玻璃仪器装入另一玻璃仪器中,经组装来完成原来需要两只或更多普通玻璃仪器进行的实验.因其具有许多优点,近年被广泛开发并应用于化学实验中.请观察下列实验装置,分析实验原理,并回答下列问题:
“套管实验”是将一支较小的玻璃仪器装入另一玻璃仪器中,经组装来完成原来需要两只或更多普通玻璃仪器进行的实验.因其具有许多优点,近年被广泛开发并应用于化学实验中.请观察下列实验装置,分析实验原理,并回答下列问题:(1)从点燃酒精灯开始,试管及烧杯A、B中能观察到的现象有
(2)整个实验结束时,在操作上需要特别注意的问题是
(3)通过该实验可以得到的结论是(结合化学方程式来说明)
考点:探究碳酸钠与碳酸氢钠的性质
专题:几种重要的金属及其化合物
分析:(1)加热时,大试管中气体受热膨胀,可以观察到烧杯A中有气泡产生;碳酸氢钠受热分解生成碳酸钠、二氧化碳和会,白色的硫酸铜与水反应生成蓝色的无水硫酸铜;碳酸氢钠分解生成的二氧化碳与澄清石灰水反应生成碳酸钙沉淀;
(2)实验结束时,为了避免发生倒吸现象,应该先撤出导管再熄灭酒精灯;
(3)根据盐酸反应现象,从碳酸钠、碳酸氢钠的稳定性、分解产物等方面解答.
(2)实验结束时,为了避免发生倒吸现象,应该先撤出导管再熄灭酒精灯;
(3)根据盐酸反应现象,从碳酸钠、碳酸氢钠的稳定性、分解产物等方面解答.
解答:
解:(1)实验开始时,大试管中的气体受热膨胀,烧杯A的导气管中会有气泡冒出;
小试管中部有沾上无水硫酸铜粉末的脱脂棉变成蓝色,试管内壁有水珠产生,
碳酸氢钠加热分解生成二氧化碳气体,二氧化碳与澄清石灰水反应生成碳酸钙沉淀,所以烧杯B中导气管中有气泡产生,澄清石灰水变浑浊,
故答案为:棉花球变蓝,B中冒气泡且石灰水变白色浑浊,刚开始时A 中有气泡产生,小试管内有液滴出现;
(2)实验结束时,在操作上要特别注意:先将导气管从A、B烧杯中取出,再停止加热,以防倒吸,
故答案为:防止倒吸(或先从两烧杯移去导气管后再移去酒精灯);
(3)根据以上反应现象可知,NaHCO3的热稳定性比Na2CO3差,NaHCO3分解有CO2和H2O产生,
故答案为:NaHCO3的热稳定性比Na2CO3差,NaHCO3分解有CO2和H2O产生.
小试管中部有沾上无水硫酸铜粉末的脱脂棉变成蓝色,试管内壁有水珠产生,
碳酸氢钠加热分解生成二氧化碳气体,二氧化碳与澄清石灰水反应生成碳酸钙沉淀,所以烧杯B中导气管中有气泡产生,澄清石灰水变浑浊,
故答案为:棉花球变蓝,B中冒气泡且石灰水变白色浑浊,刚开始时A 中有气泡产生,小试管内有液滴出现;
(2)实验结束时,在操作上要特别注意:先将导气管从A、B烧杯中取出,再停止加热,以防倒吸,
故答案为:防止倒吸(或先从两烧杯移去导气管后再移去酒精灯);
(3)根据以上反应现象可知,NaHCO3的热稳定性比Na2CO3差,NaHCO3分解有CO2和H2O产生,
故答案为:NaHCO3的热稳定性比Na2CO3差,NaHCO3分解有CO2和H2O产生.
点评:本题考查碳酸钠、碳酸氢钠性质的探究,为高频考点,题目难度中等,注意掌握碳酸钠、碳酸氢钠的化学性质,正确把握碳酸氢钠的不稳定性及实验装置的作用为解答的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验式中,没有相对分子质量就可以确定分子式的是( )
①CH3 ②CH ③CH2 ④C2H5.
①CH3 ②CH ③CH2 ④C2H5.
| A、①② | B、③④ | C、②③ | D、①④ |
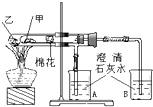 如图是某兴趣小组根据课本实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验.请观察如图实验装置、分析实验原理,并判断下列说法和做法,其中不科学的是( )
如图是某兴趣小组根据课本实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验.请观察如图实验装置、分析实验原理,并判断下列说法和做法,其中不科学的是( )| A、甲为小苏打,乙为纯碱 |
| B、整个实验过程中没有发现A烧杯的澄清石灰水变浑浊 |
| C、加热不久就能看到A烧杯的澄清石灰水变浑浊 |
| D、要证明碳酸氢钠受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球 |
将10.6g由Mg、Al、Si组成的合金投入足量的NaOH溶液中,在标准状况下产生气体11.2L;另取等质量的合金溶于过量稀H2SO4中,合金质量减少了7.8g.则合金中Mg、Al、Si的物质的量之比为( )
| A、1:2:1 |
| B、2:1:1 |
| C、1:3:2 |
| D、1:1:2 |
下列物质排放到空气中,不会使空气受到污染的是( )
| A、煤燃烧时产生的烟气 |
| B、植物光合作用产生的气体 |
| C、石油化工工厂排放的废气 |
| D、汽车排放的尾气 |
1998年出现的全球温度大幅度升高,产生了显著的“厄尓尼诺”现象,干旱和暴雨危害了许多地区.为了防止气候进一步变暖,联合国环境保护组织要求各国减少工业排放量的气体是( )
| A、SO2 |
| B、H2S |
| C、SO3 |
| D、CO2 |
 2006年6月5日是第35个世界环境日,我国环保总局确定的主题见图.下列措施不符合这一主题的是( )
2006年6月5日是第35个世界环境日,我国环保总局确定的主题见图.下列措施不符合这一主题的是( )| A、用“绿色化学”工艺,使原料尽可能转化为所需的物质 |
| B、回收废电池,减少对环境的污染 |
| C、为使农作物高产,大量施用化肥和农药 |
| D、推广垃圾分类存放,分类回收,分类处理 |
温室效应与下列气体无关的是( )
| A、二氧化碳 | B、二氧化硫 |
| C、水蒸气 | D、甲烷 |