题目内容
相同条件下,0.1mol/L Na2S2O3溶液和0.1mol/L H2SO4溶液各5mL,与10mL水混合,反应时间为t1s;0.2mol/L Na2S2O3溶液和0.2mol/L H2SO4溶液各5mL,与30mL水混合,反应时间为t2 s,则t1和t2的关系是(忽略体积变化)( )
| A、t1>t2 |
| B、t1<t2 |
| C、t1=t2 |
| D、不能肯定 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:对于Na2S2O3溶液和H2SO4溶液的反应来说,如在相同条件下进行,则物质的浓度越大,反应速率越大,可计算各物质的浓度进行比较,以此解答.
解答:
解:0.1mol/L Na2S2O3溶液和0.1mol/L H2SO4溶液各5mL,与10mL水混合,混合后c(Na2S2O3)=c(H2SO4)=
=0.025mol/L;
0.2mol/L Na2S2O3溶液和0.2mol/L H2SO4溶液各5mL,与30mL水混合,混合后c(Na2S2O3)=c(H2SO4)=
=0.025mol/L,
两溶液浓度相同,反应速率相同,则t1=t2,
故选C.
| 0.1mol/L×0.005L |
| 0.02L |
0.2mol/L Na2S2O3溶液和0.2mol/L H2SO4溶液各5mL,与30mL水混合,混合后c(Na2S2O3)=c(H2SO4)=
| 0.2mol/L×0.005L |
| 0.04L |
两溶液浓度相同,反应速率相同,则t1=t2,
故选C.
点评:本题考查化学反应速率知识,为高频考点,侧重于学生的分析能力和计算能力的考查,题目从浓度的角度考查化学反应速率的影响,注意把握比较的角度,难度不大.

练习册系列答案
相关题目
解释下列现象的离子方程式不正确的是( )
| A、铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO3-=3Fe2++2NO+4H2O |
| B、FeBr2与Cl2物质的量之比为1:1时:2Fe2++2Br-+2Cl2=2Fe3++4C1-+Br2 |
| C、向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀:A13++2SO42-+2Ba2++4OH-=2BaSO4↓+A1O2-+2H2O |
| D、漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3C1O-+3H2O=Fe(OH)3↓+3HC1O |
下列有关判断正确的是( )
| A、BaSO4(s)+4C(s)═BaS(s)+4CO(g)在试问时不能自发进行,说明该反应的△H>0 | ||
| B、常温下,水的电离程度在NH4HSO4溶液中比在纯水中大 | ||
| C、铅蓄电池放电时总反应为PbO2+Pb+2H2SO4═2PbSO4+2H2O,正、负极质量均减小 | ||
D、密闭容器中反应N2+3H2?2NH3,温度不变,增大压强,
|
从电离的角度看,下列物质不属于酸的是( )
| A、HNO3 |
| B、H2SO4 |
| C、HCl |
| D、NaHSO4 |
示意图或图示能够直观形象地呈现化学知识,下列示意图或图示正确的是( )
A、  :水分子; :水分子; :氯离子 :氯离子水合氯离子示意图 |
B、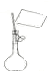 一定物质的量浓度溶液配制的某步操作 |
C、 MnO2和浓盐酸加热反应电子转移关系示意图 |
D、 丁达尔现象 |
下列各组物质中,所含分子数相同的是( )
| A、10g H2和10g O2 |
| B、标准状况时5.6L N2和44g CO2 |
| C、9g H2O和0.5mol Br2 |
| D、标准状况时224mL H2和224mL H2O |
V1mL、0.2mol/L Na2SO4溶液和V2mL、0.1mol/L Fe2(SO4)3溶液混合,已知V1大于V2,则混合溶液中SO42-的物质的量浓度可能是( )
| A、0.23 mol/L |
| B、0.18 mol/L |
| C、0.26 mol/L |
| D、0.25 mol/L |
 如图为相互串联的甲、乙两电解池.试回答:
如图为相互串联的甲、乙两电解池.试回答:


