题目内容
下列说法中正确的是( )
| A、SO2、BF3、NCl3分子中所有原子的最外层都满足8电子稳定结构 |
| B、P4和CH4都是正四面体型分子且键角都为109°28′ |
| C、NaCl晶体中与每个Na+ 距离相等且最近的Na+共有12个 |
| D、原子间通过共价键而形成的晶体一定具有高的熔、沸点及硬度 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A.分子中原子的最外层电子数可以根据每种元素原子的最外层电子数与化合价的绝对值之和来判断;
B.白磷和甲烷虽然都是正四面体结构,但是甲烷中四个H原子位于四个顶点,C原子位于四面体的中心,C-H键键角为白磷键角为109°28ˊ;白磷分子中四个P原子位于四个顶点上键角为60°;
C.根据NaCl晶体的晶胞示意图可以看出,与每个Na+距离最近且相等的Na+分布在小立方体的面对角的位置,共有12个;
D.含有共价键的晶体不一定具有高的熔、沸点及硬度,要根据晶体类型判断;
B.白磷和甲烷虽然都是正四面体结构,但是甲烷中四个H原子位于四个顶点,C原子位于四面体的中心,C-H键键角为白磷键角为109°28ˊ;白磷分子中四个P原子位于四个顶点上键角为60°;
C.根据NaCl晶体的晶胞示意图可以看出,与每个Na+距离最近且相等的Na+分布在小立方体的面对角的位置,共有12个;
D.含有共价键的晶体不一定具有高的熔、沸点及硬度,要根据晶体类型判断;
解答:
解:A.SO2中S元素化合价为+4,S原子最外层电子数为6,所以4+6=10,分子中S原子不满足8电子结构,O元素化合价为-2,O原子最外层电子数为6,所以|-2|+6=8,分子中O原子满足8电子结构;同理,CS2、NCl3中分子中所有原子的最外层都满足8电子稳定结构,故A错误;
B.白磷和甲烷都是正四面体结构,白磷键角是60°,甲烷键角是109°28ˊ,二者键角不同,故B错误;
C.与每个Na+距离最近且相等的Na+分布在小立方体的面对角的位置,共有12个,故C正确;
D.含有共价键的晶体不一定具有高的熔、沸点及硬度,如分子晶体的熔、沸点及硬度较低,故D错误;
故选C.
B.白磷和甲烷都是正四面体结构,白磷键角是60°,甲烷键角是109°28ˊ,二者键角不同,故B错误;
C.与每个Na+距离最近且相等的Na+分布在小立方体的面对角的位置,共有12个,故C正确;
D.含有共价键的晶体不一定具有高的熔、沸点及硬度,如分子晶体的熔、沸点及硬度较低,故D错误;
故选C.
点评:本题考查原子核外电子是否满足8电子稳定结构、分子结构、晶胞结构以及晶体的熔沸点,难度不大,需要注意的是P4和CH4都是正四面体型分子但键角不同.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
从电离的角度看,下列物质不属于酸的是( )
| A、HNO3 |
| B、H2SO4 |
| C、HCl |
| D、NaHSO4 |
对于2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol热化学方程式的下列说法正确的是( )
| A、.氢气与氧气反应吸收热量483.6kJ |
| B、氢气燃烧反应的燃烧热为483.6kJ |
| C、2个H2分子燃烧生成水蒸气放出483.6kJ |
| D、2molH2与1molO2生成2mol水蒸气放出483.6kJ热量 |
下列操作完成后,没有沉淀的是( )
| A、向Ca( OH)2与FeCl2混合溶液加足量稀HNO3 |
| B、向Ba( OH)2与KNO3混合溶液加足量稀H2SO4 |
| C、向AgNO3与Na2CO3混合溶液加足量稀HCl |
| D、向BaCl2与Na2CO3混合溶液中加足量AgNO3溶液 |
我省盛产矿盐(主要成分是NaCl,还含有SO42-等其他可溶性杂质的离子).下列有关说法正确的是( )
| A、有矿盐生成食盐,除去SO42- 最合适的实际是Ba(NO3)2 |
| B、工业上通过电解氯化钠溶液制备金属钠和氯气 |
| C、用酚酞试液可鉴别饱和食盐水和饱和纯碱溶液 |
| D、室温下,AgCl在水中的溶解度小于在食盐中的溶解度 |
常温下,下列两溶液:①pH=9的NaOH溶液,②pH=9的CH3COONa溶液.有关①、②两溶液,下列判断正确的是( )
| A、两溶液中水的电离程度相同,Na+的浓度不同 |
| B、两溶液分别用水稀释10倍后,有pH①<pH②<9 |
| C、①中c(Na+)与②中c(CH3COOH)相等 |
| D、将①和②等体积混合后,溶液中:c(Na+)>c(CH3COO-)=c(OH-)>c(H+) |
伞形酮可由雷梭苯乙酮和苹果酸在一定条件下反应值得
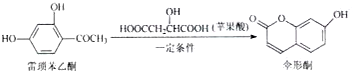
下列有关这三种物质的说法错误的是( )

下列有关这三种物质的说法错误的是( )
| A、雷梭苯乙酮有两种含氧官能团 |
| B、苹果酸和伞形酮分子中均含有1个手性碳原子 |
| C、雷梭苯乙酮和伞形酮都能跟FeCl3溶液发生显色反应 |
| D、1mol伞形酮与足量NaOH溶液反应,最多可消耗2mol NaOH |
在A2+3B2=2C的反应中,经过t秒钟后,C的浓度增加了0.6mol/L,在此期间,反应速率V(B=0.45mol/(L?S),则t值为( )
| A、1秒 | B、1.5秒 |
| C、2秒 | D、2.5秒 |



