题目内容
 甲~辛等元素在周期表中的相对位置如下表.甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素.下列判断不正确的是( )
甲~辛等元素在周期表中的相对位置如下表.甲和戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素.下列判断不正确的是( )| A、与水反应的剧烈程度:甲>乙>丁 |
| B、气态氢化物的沸点:戊<己<庚 |
| C、丙和庚的核外电子数相差15 |
| D、乙单质在空气中燃烧生成含共价键的离子化合物 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:戊的一种单质是自然界硬度最大的物质,则戊为C,甲与戊的原子序数相差3,则甲为Li、可推知乙为Na、丙为K,丁为Ca、己为Si、庚为Ge、辛为Ga.
A.根据元素的金属性强弱判断;
B.氢化物(不含氢键)相对分子质量越多,沸点越高;
C.丙为K,庚为Ge,核外电子数相差13;
D.乙单质在空气中燃烧生成生产Na2O2.
A.根据元素的金属性强弱判断;
B.氢化物(不含氢键)相对分子质量越多,沸点越高;
C.丙为K,庚为Ge,核外电子数相差13;
D.乙单质在空气中燃烧生成生产Na2O2.
解答:
解:戊的一种单质是自然界硬度最大的物质,则戊为C,甲与戊的原子序数相差3,则甲为Li、可推知乙为Na、丙为K,丁为Ca、己为Si、庚为Ge、辛为Ga.
A.金属性K>Ca>Na,元素的金属性越强,对应的单质与水反应越剧烈,故A错误;
B.戊、己、庚分别为C、Si、Ge,对应的氢化物不含氢键,相对分子质量越多,则沸点越高,故B正确;
C.丙处于第四周期第1列,庚处于第四周期第14列,第四周期每一列容纳一种元素,故二者原子序数相差13,故C错误;
D.钠在空气中燃烧生成过氧化钠,过氧化钠含有离子键、共价键,故D正确.
故选AC.
A.金属性K>Ca>Na,元素的金属性越强,对应的单质与水反应越剧烈,故A错误;
B.戊、己、庚分别为C、Si、Ge,对应的氢化物不含氢键,相对分子质量越多,则沸点越高,故B正确;
C.丙处于第四周期第1列,庚处于第四周期第14列,第四周期每一列容纳一种元素,故二者原子序数相差13,故C错误;
D.钠在空气中燃烧生成过氧化钠,过氧化钠含有离子键、共价键,故D正确.
故选AC.
点评:本题考查结构性质位置关系应用,推断元素是解题关键,注意对元素周期表的整体把握,理解同主族元素原子序数关系,难度不大.

练习册系列答案
相关题目
下列两种气体的分子数一定相等的是( )
| A、质量相等、密度不等的N2和C2H4 |
| B、等体积等密度的CO和C2H4 |
| C、等温等体积的O3和N2 |
| D、等压等体积的N2和CO2 |
除去下列溶液中的杂质(括号内是杂质)所用试剂不正确的是( )
| A、KOH溶液[K2CO3]:用Ca(OH)2溶液 |
| B、NaOH溶液[Ba(OH)2]:用Na2SO4溶液 |
| C、HNO3溶液[HCl]:用AgNO3溶液 |
| D、NaCl溶液[Na2SO4]:用Ba(NO3)2溶液 |
2005年2月18日,英国食品标准局向英国民众发出警告,公布了359种食品中含有可能致癌的“苏丹红一号”,一时间“苏丹红一号”成为媒体关注的焦点.“苏丹红一号”的结构简式如图下列关于苏丹红一号的有关叙述正确的是( )
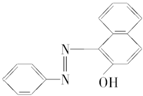

| A、苏丹红一号的分子式C18H12N2O |
| B、苏丹红一号的相对分子质量是248 g?mol-1 |
| C、苏丹红一号属于烃 |
| D、苏丹红一号能发生加成反应 |
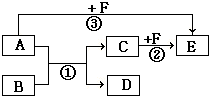 有A、B、C、D、E、F六种物质,它们之间相互转化的关系如图所示(反应条件及部分产物未标出).
有A、B、C、D、E、F六种物质,它们之间相互转化的关系如图所示(反应条件及部分产物未标出).