题目内容
1.下列各组物质,不属于同素异形体的是( )| A. | 金刚石和石墨 | B. | 白磷和红磷 | C. | Na2O和Na2O2 | D. | 氧气和臭氧 |
分析 根据同素异形体的定义判断,由同种元素组成的不同单质互称同素异形体.
解答 解:A.金刚石和石墨是由碳元素组成的不同单质,属于同素异形体,故A不选;
B.红磷和白磷是由磷元素组成的不同单质,属于同素异形体,故B不选;
C.Na2O和Na2O2是化合物,不属于同素异形体,故C选;
D.氧气与臭氧是由氧元素组成的不同单质,属于同素异形体,故D不选;
故选C.
点评 本题考查同素异形体的判断,难度不大,判断是否互为同素异形体的关键要把握两点:①同种元素形成,②不同单质,这是解决此类题的关键之所在.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.化学计量在化学中占有重要地位,请回答下列问题:
(1)在标准状况下,CO和CO2的混合气体共33.6L,质量为50g.
①两种气体总的物质的量为1.5mol.
②C与O原子个数比为3:4.
(2)实验室有一瓶失去标签的盐酸和一块镁铜合金,在0℃、1.01×105Pa时,分别向甲、乙、丙三个容器中加入100mL同浓度的盐酸后,再加入不同质量的同种粉末,得到的有关实验数据列于下表,请确定盐酸的浓度和合金的组成:
①下列的相关说法正确的是BC(填序号).
A.实验甲中,盐酸已完全反应
B.实验乙中,金属镁和盐酸恰好完全反应
C.若往实验丙的剩余物中添加盐酸,将继续产生氢气
D.金属铜参加反应并产生氢气
②盐酸的物质的量浓度4mol/L,合金中镁的质量分数27.3%.
(1)在标准状况下,CO和CO2的混合气体共33.6L,质量为50g.
①两种气体总的物质的量为1.5mol.
②C与O原子个数比为3:4.
(2)实验室有一瓶失去标签的盐酸和一块镁铜合金,在0℃、1.01×105Pa时,分别向甲、乙、丙三个容器中加入100mL同浓度的盐酸后,再加入不同质量的同种粉末,得到的有关实验数据列于下表,请确定盐酸的浓度和合金的组成:
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/g | 8.8 | 17.6 | 22.0 |
| 气体体积/L | 2.24 | 4.48 | 4.48 |
A.实验甲中,盐酸已完全反应
B.实验乙中,金属镁和盐酸恰好完全反应
C.若往实验丙的剩余物中添加盐酸,将继续产生氢气
D.金属铜参加反应并产生氢气
②盐酸的物质的量浓度4mol/L,合金中镁的质量分数27.3%.
6.下列过程中化学键未被破坏的是( )
| A. | NaCl固体溶于水 | B. | NH4Cl受热分解 | C. | 干冰升华 | D. | SO2气体溶于水 |
10.下列实验操作正确的是( )
| A. | 粗盐提纯蒸发时,待水分完全蒸干后停止加热 | |
| B. | 过滤时,漏斗下口尖端紧贴烧杯内壁 | |
| C. | 蒸馏时,冷却水应从冷凝管上口进下口出 | |
| D. | 分液操作时,上层液体应从分液漏斗下口放出 |
2.加热固体试剂时,不能使用的仪器是( )
| A. | 试管 | B. | 集气瓶 | C. | 蒸发皿 | D. | 坩埚 |
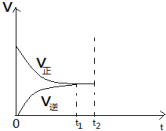 合成氨的反应中,在第一次平衡(t1时刻)后,在保持容器体积不变的情况下,在t2时刻及时分离出产物NH3,则此时平衡移动的情况是怎样的?请在图中将图补充完整.
合成氨的反应中,在第一次平衡(t1时刻)后,在保持容器体积不变的情况下,在t2时刻及时分离出产物NH3,则此时平衡移动的情况是怎样的?请在图中将图补充完整.