题目内容
8.下列分子式中只表示一种纯净物的是( )| A. | C2H4Cl2 | B. | C2H3Cl3 | C. | C2HCl3 | D. | C2H2Cl2 |
分析 纯净物是由同一种物质组成,根据分子式是否存在同分异构体进行解答.同分异构体是分子式相同,但结构不同的化合物.
解答 解:A.C2H4Cl2中2个氯原子可以连接在同一碳原子上,为1,1-二氯乙烷;每个碳原子分别连接1个氯原子,为1,2-二氯乙烷,不能表示纯净物,故A错误;
B.C2H3Cl3中3个氯原子可以连接在同一碳原子上,为1,1,1-三氯乙烷;每个碳原子分别连接1个氯原子,2个氯原子,为1,1,2-三氯乙烷,不能表示纯净物,故B错误;
C.C2HCl3只有一种结构,每个碳原子分别连接1个氯原子,2个氯原子,为1,1,2-三氯乙烯,不存在同分异构体,故C正确;
D.C2H2Cl2中2个氯原子可以连接在同一碳原子上,为1,1-二氯乙烯;每个碳原子都连接1个氯原子,为1,2-二氯乙烯,不能表示纯净物,故D错误.
故选:C.
点评 本题以纯净物为载体考查了同分异构现象,难度不大,注意纯净物必须是由同一种物质组成.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
18.柑橘是人们在日常生活中喜爱的水果之一,从柑橘中可提炼出有机物萜二烯,其结构简式为 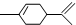 ,下列有关萜二烯的推测不正确的是( )
,下列有关萜二烯的推测不正确的是( )
 ,下列有关萜二烯的推测不正确的是( )
,下列有关萜二烯的推测不正确的是( )| A. | 萜二烯属于芳香烃 | B. | 萜二烯难溶于水 | ||
| C. | 萜二烯能发生加聚反应 | D. | 萜二烯能使酸性高锰酸钾溶液褪色 |
19.下列有机物的一氯代物只有2种的是( )
| A. |  | B. | CH3COOCH2CH3 | C. |  | D. |  |
16.下列关于氯元素的说法正确的是( )
| A. | HCl具有很强的酸性,所以氯元素的非金属性很强 | |
| B. | ${\;}_{17}^{35}$Cl、${\;}_{17}^{37}$Cl为不同的核素,有不同的化学性质 | |
| C. | 1.12LCl2含有1.7NA个质子(NA 表示阿伏加德罗常数) | |
| D. | 氯气可从KI溶液中置换出I2,说明氯的非金属性比碘强 |
3.在下列四个核反应方程中,x表示质子的是( )
| A. | ${\;}_{15}^{30}P$→${\;}_{14}^{30}Si$+x | B. | ${\;}_{7}^{14}N{+}_{0}^{1}n$→${\;}_{6}^{14}C$+x | ||
| C. | ${\;}_{27}^{60}Co$→${\;}_{28}^{60}Ni$+x | D. | ${\;}_{13}^{27}Al{+}_{2}^{4}He$→${\;}_{15}^{30}P$+x |
18.KMnO4是常见的试剂.某小组拟用酸性KMnO4溶液与H2C2O2(K2=5.4×10-2)的反应(此反应为热效反应)来探究“条件对化学反应速率的影响”并设计了如下的方案记录实验结果(忽略溶液混合体积变化)限选试剂和仪器:0.20mol/l KMnO4 溶液(酸性)蒸馏水、试管、量筒、秒表、恒温水浴槽
回答下列问题:
(1)完成上述反应原理的离子反应方程式
□MnO4-+□5H2C2O2+□6H+=□Mn2-+□CO2↑+□H2
(2)上述实验①②是温度探究对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则表格中“甲”应填写V(蒸馏水)/mL,a为1.0;乙是实验需要测量的物理量,则表格中“乙”应填
写溶液褪色的时间
(3)上述实验②④是探究催化剂对化学反应速率的影响,请在答题卷的坐标图1中画出②和④的能量变化关系图(做必要的标注)
Ⅱ某化学小组利用图2装置进行实验证明氧化性;KMnO4>Cl2>Br2,限选试剂:KBr溶液、KMnO4.浓盐酸、浓硫酸
(4)装置a、d中盛放的试剂分别是:浓盐酸、KBr溶液;试验中观察到的现象为c中有黄绿色气体产生,d中溶液变为棕黄色;此实验装置的不足之处是无尾气处理装置

| 物理量 编号 | V(0.20mol/L H2C2O4溶液)/mL | 甲 | V(O.O1mol/L KMnO4溶液)/mL | M(MnSO4固体)/g | T/℃ | 乙 |
| ① | 2.0 | 0 | 4.0 | 0 | 5.0 | |
| ② | 2.0 | 0 | 4.0 | 0 | 2.5 | |
| ③ | 1.0 | a | 4.0 | 0 | 2.5 | |
| ④ | 2.0 | 0 | 4.0 | 0.1 | 2.5 |
(1)完成上述反应原理的离子反应方程式
□MnO4-+□5H2C2O2+□6H+=□Mn2-+□CO2↑+□H2
(2)上述实验①②是温度探究对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则表格中“甲”应填写V(蒸馏水)/mL,a为1.0;乙是实验需要测量的物理量,则表格中“乙”应填
写溶液褪色的时间
(3)上述实验②④是探究催化剂对化学反应速率的影响,请在答题卷的坐标图1中画出②和④的能量变化关系图(做必要的标注)
Ⅱ某化学小组利用图2装置进行实验证明氧化性;KMnO4>Cl2>Br2,限选试剂:KBr溶液、KMnO4.浓盐酸、浓硫酸
(4)装置a、d中盛放的试剂分别是:浓盐酸、KBr溶液;试验中观察到的现象为c中有黄绿色气体产生,d中溶液变为棕黄色;此实验装置的不足之处是无尾气处理装置

19.下表是25℃时几种酸的电离平衡常数,结合相关数据和所学知识分析下列说法,其中正确的是( )
| 酸 | CH3COOH | HCN | HF | H2CO3 |
| 电离常数 | 1.8×10-5 | 4.9×10-10 | 6.6×10-4 | Ka1=4.3×10-2Ka2=5.6×10-11 |
| A. | 5种钠盐溶液pH大小关系pH(Na2CO3)>pH(NaCN)>pH(NaHCO3)>pH(CH3COONa)>pH(NaF) | |
| B. | 2mol•L-1HCN与1mol•L-1NaOH溶液等体积混合后的溶液中:c(CN-)<c(Na+)<c(HCN) | |
| C. | 向Na2CO3溶液中滴加过量的HCN溶液;2HCN+Na2CO3=2NaCN+CO2↑+H2O | |
| D. | 含等物质的量的Na2CO3、NaHCO3的混合液中:2c(Na+)=3c(CO32-)+3C(HCO3-) |
