题目内容
 (Ⅰ)多项选择题
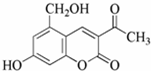
(Ⅰ)多项选择题亮菌甲素是香豆素类天然化合物,其结构简式如右图所示,下列有关亮环菌甲素的说法正确的是
A.遇FeCl3溶液显紫色
B.与Br2只能发生取代反应,不能发生加成反应
C.与足量NaOH溶液共煮时,1mol亮环菌甲素最多消耗3mol NaOH
D.滴入酸性KMnO4溶液,观察到紫红色褪去,可证明分子中存在碳碳双键
(Ⅱ)有机物F商品名称“敌稗(Propanil)”,是一种优良的水稻除草剂,现通过下列合成路线制备:

已知:
Ⅰ.RX
| NaCN |
| H2O |
Ⅱ.

Ⅲ.当一取代苯继续发生取代反应时,新引进的取代基受到原取代基的影响而取代邻位、对位或间位.使新的取代基进入它的邻位、对位的取代基:-CH3、-NH2、-X;使新的取代基进入它的间位的取代基有:-COOH、-NO2等.
请结合上述所给信息,回答问题:
(1)A的结构简式为
(2)反应②的化学反应方程式:
(3)有人认为:若将②、③两步反应顺序颠倒,也可以得到C,实际上是不妥的.请你指出不妥之处
(4)反应⑤的化学反应方程式:
(5)符合下列条件的F的同分异构体有
①两个氯原子和氨基直接与苯环相连;
②苯环上核磁共振氢谱为单峰;
(6)请你设计D→E(C3H6O2)的合成路线.
要求:①合成过程中无机试剂任选、有机原料为碳原子不超过2个的烃;
②合成反应流程图表示方法示例如下:A
| 反应物 |
| 反应条件 |
| 反应物 |
| 反应条件 |
考点:有机物的合成,有机物的结构和性质
专题:有机物的化学性质及推断
分析:(Ⅰ)亮菌甲素中有酚羟基、醇羟基、碳碳双键、羰基、酯基等官能团,根据官能团的性质判断;
(Ⅱ)根据反应③结合已知Ⅱ可推知C为 ,根据已知Ⅲ可推知B为
,根据已知Ⅲ可推知B为 ,A为
,A为 ,E呈酸性,结合E的分子式可知,E应为CH3CH2COOH,由E和反应⑤可推知F为
,E呈酸性,结合E的分子式可知,E应为CH3CH2COOH,由E和反应⑤可推知F为 ,有机原料碳原子不超过2个,应以为原料CH2=CH2,结合已知Ⅰ,经过加成、取代后生成CH3CH2CN,经水解可生成CH3CH2COOH,据此答题.
,有机原料碳原子不超过2个,应以为原料CH2=CH2,结合已知Ⅰ,经过加成、取代后生成CH3CH2CN,经水解可生成CH3CH2COOH,据此答题.
(Ⅱ)根据反应③结合已知Ⅱ可推知C为
 ,根据已知Ⅲ可推知B为
,根据已知Ⅲ可推知B为 ,A为
,A为 ,E呈酸性,结合E的分子式可知,E应为CH3CH2COOH,由E和反应⑤可推知F为
,E呈酸性,结合E的分子式可知,E应为CH3CH2COOH,由E和反应⑤可推知F为 ,有机原料碳原子不超过2个,应以为原料CH2=CH2,结合已知Ⅰ,经过加成、取代后生成CH3CH2CN,经水解可生成CH3CH2COOH,据此答题.
,有机原料碳原子不超过2个,应以为原料CH2=CH2,结合已知Ⅰ,经过加成、取代后生成CH3CH2CN,经水解可生成CH3CH2COOH,据此答题.解答:
解:(Ⅰ)亮菌甲素中有酚羟基、醇羟基、碳碳双键、羰基、酯基等官能团,
A.有酚羟基,所以遇FeCl3溶液显紫色,故A正确;
B.有碳碳双键,与Br2能发生加成反应,故B错误;
C.有酚羟基和一个酯基,酯基水解后可生成酚羟基,所以与足量NaOH溶液共煮时,1mol亮环菌甲素最多消耗3mol NaOH,故C正确;
D.酚羟基、醇羟基等都能使高锰酸钾溶液褪色,所以滴入酸性KMnO4溶液,观察到紫红色褪去,不能证明分子中存在碳碳双键,故D错误;
故选AC;
(Ⅱ)根据反应③结合已知Ⅱ可推知C为 ,根据已知Ⅲ可推知B为
,根据已知Ⅲ可推知B为 ,A为
,A为 ,E呈酸性,结合E的分子式可知,E应为CH3CH2COOH,由E和反应⑤可推知F为
,E呈酸性,结合E的分子式可知,E应为CH3CH2COOH,由E和反应⑤可推知F为 ,有机原料碳原子不超过2个,应以为原料CH2=CH2,结合已知Ⅰ,经过加成、取代后生成CH3CH2CN,经水解可生成CH3CH2COOH,
,有机原料碳原子不超过2个,应以为原料CH2=CH2,结合已知Ⅰ,经过加成、取代后生成CH3CH2CN,经水解可生成CH3CH2COOH,
(1)根据上面的分析可知,A的结构简式为 ,其结构中有3种不同化学环境的氢;B为
,其结构中有3种不同化学环境的氢;B为 ,B中含氧官能团的名称是硝基,
,B中含氧官能团的名称是硝基,
故答案为: ;3;
;3; ;
;
(2)苯和氯气发生取代反应后生成 ,
, 与氯气在催化作用下取代,在邻位上引入-Cl,方程式为
与氯气在催化作用下取代,在邻位上引入-Cl,方程式为 ,
,
故答案为: ;
;
(3)若②③两步反应颠倒,则不能在-Cl的对位引入-NO2,所以二者不可以颠倒,防止所得C的纯度不高,
故答案为:所得C的纯度不高;
(4)反应⑤为 与CH3CH2COOH的取代反应,方程式为
与CH3CH2COOH的取代反应,方程式为 ,
,
故答案为: ;
;
(5)F为 ,符合下列条件①两个氯原子和氨基直接与苯环相连;②苯环上核磁共振氢谱为单峰,F的同分异构体为
,符合下列条件①两个氯原子和氨基直接与苯环相连;②苯环上核磁共振氢谱为单峰,F的同分异构体为 或
或 ,其中-C3H5O的结构有-CH2CH2CHO、-CH2COCH3、-COCH2CH3、-CH(CH3)CHO、-CH=CHCH2OH、-CH(OH)CH=CH2六种结构,所以同分异构体共有12种,
,其中-C3H5O的结构有-CH2CH2CHO、-CH2COCH3、-COCH2CH3、-CH(CH3)CHO、-CH=CHCH2OH、-CH(OH)CH=CH2六种结构,所以同分异构体共有12种,
故答案为:12;
(6)根据题给信息,要制备CH3CH2COOH,可先制备CH3CH2CN,CH3CH2CN可由CH3CH2Br取代生成,而CH3CH2Br可由CH2=CH2加成生成,则反应流程为CH2=CH2
CH3CH2Br
CH3CH2CN
CH3CH2COOH,
故答案为:CH2=CH2
CH3CH2Br
CH3CH2CN
CH3CH2COOH.
A.有酚羟基,所以遇FeCl3溶液显紫色,故A正确;
B.有碳碳双键,与Br2能发生加成反应,故B错误;
C.有酚羟基和一个酯基,酯基水解后可生成酚羟基,所以与足量NaOH溶液共煮时,1mol亮环菌甲素最多消耗3mol NaOH,故C正确;
D.酚羟基、醇羟基等都能使高锰酸钾溶液褪色,所以滴入酸性KMnO4溶液,观察到紫红色褪去,不能证明分子中存在碳碳双键,故D错误;
故选AC;
(Ⅱ)根据反应③结合已知Ⅱ可推知C为
 ,根据已知Ⅲ可推知B为
,根据已知Ⅲ可推知B为 ,A为
,A为 ,E呈酸性,结合E的分子式可知,E应为CH3CH2COOH,由E和反应⑤可推知F为
,E呈酸性,结合E的分子式可知,E应为CH3CH2COOH,由E和反应⑤可推知F为 ,有机原料碳原子不超过2个,应以为原料CH2=CH2,结合已知Ⅰ,经过加成、取代后生成CH3CH2CN,经水解可生成CH3CH2COOH,
,有机原料碳原子不超过2个,应以为原料CH2=CH2,结合已知Ⅰ,经过加成、取代后生成CH3CH2CN,经水解可生成CH3CH2COOH,(1)根据上面的分析可知,A的结构简式为
 ,其结构中有3种不同化学环境的氢;B为
,其结构中有3种不同化学环境的氢;B为 ,B中含氧官能团的名称是硝基,
,B中含氧官能团的名称是硝基,故答案为:
 ;3;
;3; ;
;(2)苯和氯气发生取代反应后生成
 ,
, 与氯气在催化作用下取代,在邻位上引入-Cl,方程式为
与氯气在催化作用下取代,在邻位上引入-Cl,方程式为 ,
,故答案为:
 ;
;(3)若②③两步反应颠倒,则不能在-Cl的对位引入-NO2,所以二者不可以颠倒,防止所得C的纯度不高,
故答案为:所得C的纯度不高;
(4)反应⑤为
 与CH3CH2COOH的取代反应,方程式为
与CH3CH2COOH的取代反应,方程式为 ,
,故答案为:
 ;
;(5)F为
 ,符合下列条件①两个氯原子和氨基直接与苯环相连;②苯环上核磁共振氢谱为单峰,F的同分异构体为
,符合下列条件①两个氯原子和氨基直接与苯环相连;②苯环上核磁共振氢谱为单峰,F的同分异构体为 或
或 ,其中-C3H5O的结构有-CH2CH2CHO、-CH2COCH3、-COCH2CH3、-CH(CH3)CHO、-CH=CHCH2OH、-CH(OH)CH=CH2六种结构,所以同分异构体共有12种,
,其中-C3H5O的结构有-CH2CH2CHO、-CH2COCH3、-COCH2CH3、-CH(CH3)CHO、-CH=CHCH2OH、-CH(OH)CH=CH2六种结构,所以同分异构体共有12种,故答案为:12;
(6)根据题给信息,要制备CH3CH2COOH,可先制备CH3CH2CN,CH3CH2CN可由CH3CH2Br取代生成,而CH3CH2Br可由CH2=CH2加成生成,则反应流程为CH2=CH2
| HBr |
| 催化剂 |
| NaCN |
| H2O |
故答案为:CH2=CH2
| HBr |
| 催化剂 |
| NaCN |
| H2O |
点评:本题考查有机物的合成,题目难度中等,解题的关键是能把握题给信息,注意把握有机物的结构和性质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
等质量的下列有机物完全燃烧,消耗O2最多的是( )
| A、乙烯(C2H4) |
| B、乙烷 |
| C、丙烷 |
| D、异丁烷 |
下列不能说明氯的非金属性比硫强的事实是( )
①HCl比H2S稳定
②HCl和H2S的水溶液前者的酸性强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl原子能得1个电子变成稳定离子而S原子能得两个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
①HCl比H2S稳定
②HCl和H2S的水溶液前者的酸性强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl原子能得1个电子变成稳定离子而S原子能得两个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
| A、①②④ | B、①②⑥ |
| C、②⑤ | D、①③⑤ |
下列关于甲烷的叙述正确的是( )
| A、甲烷不能使酸性高锰酸钾溶液退色,所以,甲烷不能被氧化 |
| B、甲烷可以与氯气发生取代反应,因此,可以使氯水褪色 |
| C、甲烷能够燃烧,在一定条件下会发生爆炸,因此,是矿井安全的重要威胁之一 |
| D、将甲烷与氯气以体积比为1:1的比例混合,光照条件下就可得到比较纯净的CH3Cl |
 X是一种天然有机物,其结构简式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是重要的有机合成原料.下列关于物质X的说法正确的是 ( )
X是一种天然有机物,其结构简式如图所示,常被用于香料或作为饮料的酸化剂,在食品和医学上用作多价螯合剂,也是重要的有机合成原料.下列关于物质X的说法正确的是 ( )| A、X不能发生消去反应 |
| B、1 mol物质X可以和4 mol NaOH反应 |
| C、X的核磁共振氢谱中有6个峰 |
| D、等物质的量的X分别与足量的Na、NaHCO3反应得到的气体物质的量后者大 |
若用NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
| A、46 g C2H6O中共用电子对数为8NA |
| B、20 g重水(D2O)中含有的电子数为10NA |
| C、100 mL 2.0 mol?L-1 NH4HCO3溶液中NH4+数为0.2NA |
| D、标准状况下,22.4 L NO与CO的混合气体中含有的原子数为2NA |

 的合成路线(合成路线常用的表示方法为:A
的合成路线(合成路线常用的表示方法为:A 碳是形成化合物种类最多的元素.
碳是形成化合物种类最多的元素.