题目内容
11.30g由14C2H2和C18O组成的混合气体中含有的质子数为14NA.分析 14C2H2和C18O的摩尔质量均为30g/mol,故求出30g14C2H2和C18O混合气体的物质的量,然后根据14C2H2和C18O中均含14个质子来分析计算.
解答 解:14C2H2和C18O的摩尔质量均为30g/mol,故30g14C2H2和C18O混合气体的物质的量n=$\frac{30g}{30g/mol}$=1mol,与两者的比例无关,而14C2H2和C18O中均含14个质子,故1mol混合物中含有14mol质子即14NA个,与两者的比例无关.
答:正确.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
1.某小组同学利用图所示装置进行铁的电化学腐蚀原理的探究实验:
(l)小组同学认为以上两种检验方法,均能证明铁发生了电化学腐蚀.
①实验i中的现象是碳棒附近溶液变红.
②用化学用语解释实验i中的现象:O2+2H2O+4e-═4OH-.
(2)查阅资料:K3[Fe(CN)6]具有氧化性.
①据此有同学认为仪通过ii中现象不能证明铁发生了电化学腐蚀,理由是铁电极能直接和K3[Fe(CN)6]溶液发生氧化还原反应生成Fe2+,会干扰由于电化学腐蚀负极生成Fe2+的检验
②进行下列实验,在实验几分钟后的记录如表:
a.以上实验表明:在Cl-存在条件下,K3[Fe(CN)6]溶液可以与铁片发生反应.
b.为探究Cl-的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验III,发现铁片表面产生蓝色沉淀.此补充实验表明Cl-的作用是Cl-破坏了铁表面的氧化膜.
(3)有同学认为上述实验仍不严谨.为进一步探究K3[Fe(CN)6]的氧化性对实验ii结果的影响,又利用(2)中装置继续实验.其中能证实以上影响确实存在的是AC(填字母序号).
(4)综合以上实验分析,利用实验ii中试剂能证实铁发生了电化学腐蚀的实验方案是取出少许铁片(负极)附近的溶液于试管中,滴加K3[Fe(CN)6]溶液,若出现蓝色沉淀,则说明负极附近溶液中产生了Fe2+,即发生了电化学腐蚀.
| 装置 | 分别进行的实验 | 现象 |
 | i.连好装置 一段时间后,向烧杯中滴加酚酞 | 碳棒附近溶液变红 |
| ii.连好装置 一段时间后,向烧杯中滴加[K3[Fe(CN)6] | 铁片表面产生蓝色沉淀 |
①实验i中的现象是碳棒附近溶液变红.
②用化学用语解释实验i中的现象:O2+2H2O+4e-═4OH-.
(2)查阅资料:K3[Fe(CN)6]具有氧化性.
①据此有同学认为仪通过ii中现象不能证明铁发生了电化学腐蚀,理由是铁电极能直接和K3[Fe(CN)6]溶液发生氧化还原反应生成Fe2+,会干扰由于电化学腐蚀负极生成Fe2+的检验
②进行下列实验,在实验几分钟后的记录如表:
| 实验 | 滴加 | 试管 | 现象 |
 | 0.5mol.LK3[Fe(CN)6]溶液 | iii.蒸馏水 | 无明显变化 |
| iv.1.0mol•L-1NaCl溶液 | 铁片表面产生大量蓝色沉淀 | ||
| v.0.5mol•L-1Na2SO4溶液 | 无明显变化 |
b.为探究Cl-的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验III,发现铁片表面产生蓝色沉淀.此补充实验表明Cl-的作用是Cl-破坏了铁表面的氧化膜.
(3)有同学认为上述实验仍不严谨.为进一步探究K3[Fe(CN)6]的氧化性对实验ii结果的影响,又利用(2)中装置继续实验.其中能证实以上影响确实存在的是AC(填字母序号).
| 实验 | 试剂 | 现象 |
| A | 酸洗后的铁片K3[Fe(CN)6]溶液(已除O2) | 产生蓝色沉淀 |
| B | 酸洗后的铁片K3[Fe(CN)6]和NaCl混合溶液(未除O2) | 产生蓝色沉淀 |
| C | 铁片K3[Fe(CN)6]和NaCl混合溶液(已除O2) | 产生蓝色沉淀 |
| D | 铁片K3[Fe(CN)6]和盐酸混合溶液(已除O2) | 产生蓝色沉淀 |
2.对四支分别盛有无色溶液的试管,进行如下操作,结论正确的是( )
| 操作 | 现象 | 结论 | |
| A | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫红色 | 原溶液中有I- |
| B | 滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中一定有SO42- |
| C | 向10mL 0.2mol/LNaOH溶液中先滴入2滴0.1mol/LMgCl2溶液,再滴加2滴0.1mol/LFeCl3溶液 | 先有白色沉淀生成,加入FeCl3溶液后,又有红褐色沉淀生成 | 在相同的温度下的Ksp:Mg(OH)2>Fe(OH)3 |
| D | 滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中一定无NH4+ |
| A. | A | B. | B | C. | C | D. | D |
19.下列关于有机化合物的说法正确的是( )
| A. | C2H6和C3H8不存在同分异构体,CH2O和C2H4O2互为同系物 | |
| B. | 一定条件下,乙烯、乙酸乙酯和淀粉都能与水反应 | |
| C. | 乙烯和苯分子中都含有碳碳双键,都能使溴水褪色 | |
| D. | 糖类、油脂和蛋白质都能发生水解 |
16. 短周期元素R、T、Q、W、G在元素周期表中的相对位置如下表所示,其中Q是无机非金属材料的主角.下列判断正确的是( )
短周期元素R、T、Q、W、G在元素周期表中的相对位置如下表所示,其中Q是无机非金属材料的主角.下列判断正确的是( )
 短周期元素R、T、Q、W、G在元素周期表中的相对位置如下表所示,其中Q是无机非金属材料的主角.下列判断正确的是( )
短周期元素R、T、Q、W、G在元素周期表中的相对位置如下表所示,其中Q是无机非金属材料的主角.下列判断正确的是( )| A. | 离子半径:T<W<G | |
| B. | 等物质的量的W、G单质分别与足量铁粉反应,前者消耗的铁粉多 | |
| C. | 最简单气态氢化物的热稳定性:Q>R | |
| D. | 工业上通过电解T和G组成的化合物冶炼T的单质 |
3.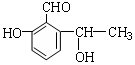 某有机物的结构简式如图,它可能发生的反应类型有( )
某有机物的结构简式如图,它可能发生的反应类型有( )
①取代 ②加成 ③消去 ④水解⑤酯化 ⑥中和 ⑦氧化 ⑧加聚.
 某有机物的结构简式如图,它可能发生的反应类型有( )
某有机物的结构简式如图,它可能发生的反应类型有( )①取代 ②加成 ③消去 ④水解⑤酯化 ⑥中和 ⑦氧化 ⑧加聚.
| A. | ①②③④⑥ | B. | ②③④⑤⑧ | C. | ③④⑤⑥⑦ | D. | ①②③⑤⑥⑦ |
12.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) | |
| B. | 0.1 mol/L NH4Cl溶液:c(NH4+ )=c(Cl-) | |
| C. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 0.1mol AgCl和0.1molAgI混合后加入100mL水中,所得溶液中c(Cl-)=c(I-) |
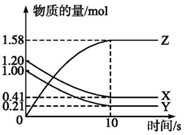 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示: