题目内容
12.下列各溶液中,微粒的物质的量浓度关系正确的是( )| A. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) | |
| B. | 0.1 mol/L NH4Cl溶液:c(NH4+ )=c(Cl-) | |
| C. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 0.1mol AgCl和0.1molAgI混合后加入100mL水中,所得溶液中c(Cl-)=c(I-) |
分析 A.硝酸钠为强酸强碱盐,且与盐酸不反应;
B.氯化铵为强酸弱碱盐,铵根离子水解;
C.得到的酸性混合溶液,可知c(H+)>c(OH-),结合电荷守恒式c(Na+)+c(H+)=c(CH3COO-)+c(OH-)分析;
D.AgI的溶解度小于AgCl的溶解度.
解答 解:A.硝酸钠为强酸强碱盐,且与盐酸不反应,则混合溶液中c(Na+)=c(NO3-),与pH=5无关,故A正确;
B.氯化铵为强酸弱碱盐,铵根离子水解导致其离子浓度减小,则0.1 mol/L NH4Cl溶液:c(NH4+ )<c(Cl-),故B错误;
C.得到的酸性混合溶液,可知c(H+)>c(OH-),由c(Na+)+c(H+)=c(CH3COO-)+c(OH-)可知,c(Na+)<c(CH3COO-),故C错误;
D.AgI的溶解度小于AgCl的溶解度,则0.1mol AgCl和0.1molAgI混合后加入100mL水中,所得溶液中c(Cl-)>c(I-),故D错误;
故选A.
点评 本题考查离子浓度大小的比较,为高频考点,把握盐类水解、电荷守恒、难溶电解质的溶解度为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列物质中所含分子数最多的是( )
| A. | 56 g N2 | B. | 3.01×1023个硫酸分子 | ||
| C. | 标准状况下 22.4 LCl2 | D. | 1.5 molO2 |
7.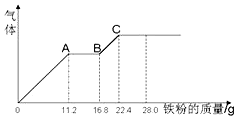 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )| A. | 原溶液中H2SO4浓度为4mol•L-1 | |
| B. | 图中,AB段的反应为2Fe3++Fe=3Fe2+,A点的溶质为Fe(NO3)3 | |
| C. | 原混合液中NO3-的物质的量为0.4mol | |
| D. | 图中,OA段产生是NO,BC段产生的气体是氢气 |
4.下列氧化还原反应所标出的电子转移情况中没有错误的是( )
| A. |  | |
| B. |  | |
| C. |  | |
| D. |  |
1.下列物质的溶液长期暴露在空气中会变质而溶液又会出现白色浑浊的是( )
| A. | NaHCO3 | B. | FeCl2 | C. | KI | D. | Na 2SiO 3 |
2.下列变化中可以说明SO2具有漂白性的是( )
| A. | SO2通入酸性高锰酸钾溶液中红色褪去 | |
| B. | SO2通入品红溶液红色褪去 | |
| C. | SO2通入溴水溶液中红棕色褪去 | |
| D. | SO2通入氢氧化钠与酚酞的混合溶液红色褪去 |

 .
.