题目内容
17.下列除杂方案正确的是(括号内为除杂剂)( )| A. | CO2中混有CO (炽热的炭) | B. | NaOH溶液中混有Ba(OH)2(CuSO4) | ||
| C. | CO2中混有HCl气体 (NaOH溶液) | D. | Cu(NO3)2中混有AgNO3(Cu粉) |
分析 A.二氧化碳与碳反应;
B.生成氢氧化铜,消耗氢氧化钠;
C.二者都与氢氧化钠溶液反应;
D.铜比银活泼,可置换出银.
解答 解:A.二氧化碳与碳反应,应用CuO除杂,故A错误;
B.氢氧化钠与硫酸铜反应,消耗氢氧化钠,可用硫酸钠除杂,故B错误;
C.二者都与氢氧化钠溶液反应,一般用饱和碳酸氢钠溶液除杂,故C错误;
D.铜比银活泼,可置换出银,可用于除杂,故D正确.
故选D.
点评 本题考查混合物分离提纯,为高频考点,注意把握物质的性质、性质差异及混合物分离方法,特别注意除杂时不能引入新杂质,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
3. 向FeCl3、CuCl2混合溶液中通入H2S和O2的混合气体可回收S,其转化关系如图.相关说法不正确的是( )
向FeCl3、CuCl2混合溶液中通入H2S和O2的混合气体可回收S,其转化关系如图.相关说法不正确的是( )
 向FeCl3、CuCl2混合溶液中通入H2S和O2的混合气体可回收S,其转化关系如图.相关说法不正确的是( )
向FeCl3、CuCl2混合溶液中通入H2S和O2的混合气体可回收S,其转化关系如图.相关说法不正确的是( )| A. | 反应I的基本反应类型是复分解反应 | |
| B. | 反应II中每生成1molS需要2molFeCl3 | |
| C. | 在转化过程中能循环利用的物质有FeCl2和CuCl2 | |
| D. | 在转化过程中化合价不变的元素只有Cu和Cl |
8.太空探索器常用${\;}_{94}^{238}$Pu制成的核电池提供动力,该钚原子的中子数为( )
| A. | 332 | B. | 238 | C. | 144 | D. | 94 |
5.短周期主族元素X、Y、Z、W的原子序数依次增大,四种元素的原子K层电子数总和为7,L层电子数总和为22,M层电子数总和为12.下列说法正确的是( )
| A. | 最高正价由低到高的顺序为:X、Z、Y、W | |
| B. | 原子半径由小到大的顺序为:X、Y、Z、W | |
| C. | 最外层电子数由少到多的顺序为:X、Z、Y、W | |
| D. | 简单氢化物的稳定性由弱到强的顺序为:Y、Z、W |
12.下列实验中,所采取的分离方法与对应原理都正确的是( )
| 选项 | 实验目的 | 分离方法 | 原理 |
| A | 除去CO2中的HCl | 通入饱和Na2CO3溶液 | HCl和Na2CO3溶液反应生成CO2 |
| B | 除去乙醇中少量的乙酸 | 加入足量生石灰蒸馏 | 乙醇和乙酸钙的沸点相差较大 |
| C | 除去KNO3固体中NaCl | 冷却热饱和溶液重结晶 | NaCl在水中的溶解度很大 |
| D | 分离乙酸和乙醇 | 用分液漏斗分液 | 乙醇乙酯和乙醇的密度不同 |
| A. | A | B. | B | C. | C | D. | D |
2.根据下表信息回答以下问题:
部分短周期元素的原子半径及主要化合价
(1)将A、D、E、F、H对应的简单离子按照半径由小到大的顺序填空Mg2+<Na+<O2-<Cl-<S2-.
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是Al(OH)3+3H+=Al3++3H2O.
(3)实验室中制取H单质反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
| 元素 | A | B | C | D | E | F | G | H |
| 原子半径(nm) | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 | 0.154 | 0.037 | 0.099 |
| 主要化合价 | +2 | +3 | +2 | +6,-2 | -2 | +1 | +1 | +7,-1 |
(1)将A、D、E、F、H对应的简单离子按照半径由小到大的顺序填空Mg2+<Na+<O2-<Cl-<S2-.
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是Al(OH)3+3H+=Al3++3H2O.
(3)实验室中制取H单质反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
9.如图所示装置可用于(需要时可以用酒精灯加热)( )
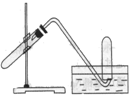

| A. | 加热NaHCO3制取和收集CO2 | |
| B. | 用铜和稀硝酸反应制取和收集NO | |
| C. | 用NH4Cl与浓NaOH溶液反应制取和收集NH3 | |
| D. | 用铜和浓硝酸反应制取和收集NO2 |
6.下列说法正确的是( )
| A. | pH=6的纯水中,c(OH-)=10-8 mol•L-1 | |
| B. | 向0.1 mol•L-1Na2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32-)均增大 | |
| C. | 室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后溶液pH>7 | |
| D. | 0.1 mol•L-1Na2CO3溶液中c(OH-)=c(H+)+c(HCO3-)+c(H2CO3) |
7.铝分别与足量的稀盐酸和NaOH溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗HCl和NaOH的物质的量之比为( )
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 4:1 |