题目内容
11.下列有关说法正确的是( )| A. | 2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物种类数相同 | |
| B. | 乙烷、苯、裂化汽油溶液均不能使酸性高锰酸钾溶液褪色 | |
| C. | 苯的密度比水小,但由苯反应制得的溴苯、硝基苯、环已烷的密度都比水大 | |
| D. | 乙酸乙酯在碱性条件下的水解反应称为皂化反应 |
分析 A.烷烃中含有几种等效氢原子,则一氯代物有几种;
B.裂化汽油能使酸性高锰酸钾溶液褪色;
C.环己烷的密度比水的小;
D.油脂在碱性条件下的水解反应称为皂化反应.
解答 解:A.2,2-二甲基丁烷中含有3种等效氢原子,则一氯代物有3种,2,4-二甲基戊烷中含有3种等效氢原子,则一氯代物也有3种,故A正确;
B.乙烷、苯不能使酸性高锰酸钾溶液褪色,裂化汽油能使酸性高锰酸钾溶液褪色,故B错误;
C.苯的密度比水小,但由苯反应制得的溴苯、硝基苯的密度都比水的大,但环己烷的密度比水的小,故C错误;
D.油脂在碱性条件下水解生成高级脂肪酸钠和甘油,称为皂化反应,故D错误;
故选A.
点评 本题主要考查的是同分异构体的判断、常见有机化合物的性质等,综合性较强,把握官能团与性质的关系为解答的关键,题目难度不大.

练习册系列答案
相关题目
9.已知醋酸与氢氧化钠在溶液中发生下列反应①,醋酸钠在溶液中又能跟水发生下列反应②.
①CH3COOH+Na0H=CH3COONa+H20
②CH3COONa+H20?CH3COOH+Na0H
上述化学方程式①和②可合并写为
③CH3COOH+Na0H=CH3COONa+H20
下列叙述正确的是( )
①CH3COOH+Na0H=CH3COONa+H20
②CH3COONa+H20?CH3COOH+Na0H
上述化学方程式①和②可合并写为
③CH3COOH+Na0H=CH3COONa+H20
下列叙述正确的是( )
| A. | 反应①和②都是离子反应 | B. | 反应①和②都吸收热量 | ||
| C. | 反应①和②都放出热量 | D. | 反应③既不吸收热量也不放出热量 |
2.配制一定物质的量浓度的溶液时,由于操作不慎,使得液面略超过容量瓶的刻度(标线),这时应采取的措施是( )
| A. | 再加点溶质到容量瓶中去 | B. | 影响不大,不再处理 | ||
| C. | 用胶头滴管准确吸出标线上的溶液 | D. | 重新配制 |
19.下列有关说法或表示正确的是( )
| A. | 淀粉和纤维素都可用(C6H10O5)n表示,二者互为同分异构体 | |
| B. | Mg5(Si4O10)2(OH)2•4H2O的氧化物形式:5MgO•8SiO2•5H2O | |
| C. | Fe-2e-=Fe2+可表示钢铁析氢腐蚀和吸氧腐蚀的正极反应 | |
| D. | 乙醇分子的比例模型: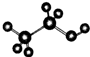 |
6.下列关于阿伏加德罗常数NA的说法正确的是( )
| A. | 8g CH4所含共价键数目为2NA | |
| B. | 0.5NA 个氯气分子与水反应转移电子数为0.5NA | |
| C. | 50mL12mol/L盐酸与足量的MnO2共热,转移的电子数为0.3NA | |
| D. | 1 L0.2mol/L的Na2S溶液中离子数为0.6NA |
3.瓦斯中CH4与O2的质量比为1:4时极易爆炸,此时它们的体积比为( )
| A. | 1:4 | B. | 1:3 | C. | 1:2 | D. | 1:1 |
20.下列实验操作中正确的是( )
| A. | 萃取操作时,可以选用CCl4或酒精作为萃取剂从碘水中萃取碘 | |
| B. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| C. | 分液操作时,下层液体从分液漏斗下口放出,上层液体从下口放出到另一个烧杯中 | |
| D. | 蒸馏操作时,收集完馏分后,先停止加热,待恢复室温后再停止通冷凝水 |
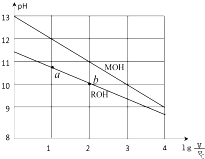 室温下,将浓度均为0.10mol/L体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随$lg\frac{V}{V_0}$的变化如图所示,下列叙述错误的是( )
室温下,将浓度均为0.10mol/L体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随$lg\frac{V}{V_0}$的变化如图所示,下列叙述错误的是( )