��Ŀ����
8�� ij��ѧ��ȤС��Ϊ̽��Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�飮
ij��ѧ��ȤС��Ϊ̽��Ԫ�����ʵĵݱ���ɣ����������ϵ��ʵ�飮��1�����ơ��ء�þ������1mol�ֱ�Ͷ�뵽������0.1mol•L-1�������У���Ԥ��ʵ������K�����ᷴӦ����ң�Al�����ᷴӦ������
��2����NaOH��Һ��NH4Cl��Һ�������NH3•H2O���Ӷ���֤NaOH�ļ��Դ���NH3•H2O���̶�������֤Na�Ľ����Դ���N������Ϊ������Ƿ��������������˵�����ɣ��ü���ǿ���ȽϽ�����ǿ��ʱ��һ��Ҫ��Ԫ�ص�����������ˮ����ļ���ǿ���Ƚϣ���NH3•H2O���ǵ�Ԫ�ص�����������ˮ���
��������ͼװ�ÿ�����֤�ǽ����Եı仯���ɣ�
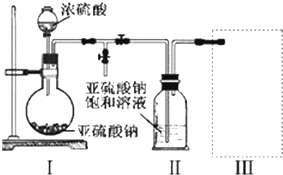
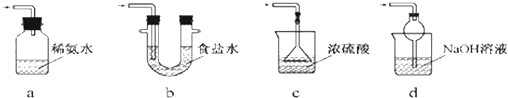
��3������A������Ϊ��Һ©���������D�������Ƿ�ֹ������
��4��ʵ����������ҩƷNa2S��KMnO4��Ũ���ᡢMnO2����������ѡ�����ҩƷ���ʵ����֤�ȵķǽ����Դ�����װ��A��B��C����װҩƷ�ֱ�ΪŨ���ᡢKMnO4��Na2S��װ��C�е�ʵ������Ϊ�е���ɫ�������ɣ����ӷ���ʽΪS2-+Cl2�TS��+2Cl-��
��5����Ҫ֤���ǽ����ԣ�C��Si���������ѧ����֪ʶѡ����Ӧ���Լ�����A�м����ᡢB�м�Na2CO3��C�м�Na2SiO3���۲쵽C����Һ������Ϊ�а�ɫ��״����������
���� I����1��Ԫ�صĽ�����Խǿ���䵥�������ˮ��ӦԽ���ң�
��2��Ԫ�ص�����������ˮ����ļ���Խǿ��Ԫ�صĽ�����Խǿ��
II����3�����������Ĺ���д������A�����ƣ����θ���ܾ��з�ֹ���������ã�
��4�����ʵ����֤�ǽ����ԣ�Cl��S������������Na2S��������ԭ��Ӧ����֤��
��5��Ҫ֤���ǽ����ԣ�C��Si������ͨ��������̼�����Ʒ�Ӧ���������ԵĹ�����֤����
��� �⣺I����1��ͬһ����Ԫ�أ�����������ԭ�����������������Ԫ�صĽ�����Խǿ��ͬһ���壬ԭ������Խ������Խǿ���䵥�������ˮ��ӦԽ���ң����Խ�����K��Na��Mg��Al����K�����ᷴӦ����ҡ�Al�����ᷴӦ�����������ʴ�Ϊ��K��Al��
��2����NaOH��Һ��NH4Cl��Һ�������NH3•H2O������˵��NaOH�ļ��Դ���NH3•H2O��������˵��Na�Ľ����Դ���N����ΪҪ��֤�����Ե�ǿ��������ͨ���Ƚ��������������Ӧ��ˮ����ļ��������бȽϣ���NH3•H2O���ǵ�Ԫ�ص�����������ˮ���
�ʴ�Ϊ�����������ü���ǿ���ȽϽ�����ǿ��ʱ��һ��Ҫ��Ԫ�ص�����������ˮ����ļ���ǿ���Ƚϣ���NH3•H2O���ǵ�Ԫ�ص�����������ˮ���
II����3������AΪ��Һ©�������θ����D�ܹ���ֹ���������Ա���C��Һ�������ƿ�У��ʴ�Ϊ����Һ©������ֹ������
��4�����ʵ����֤�ǽ����ԣ�Cl��S������������Na2S��������ԭ��Ӧ����֤����װ��A��B��C����װҩƷӦ�ֱ�ΪŨ���ᡢKMnO4��Na2S��Һ��װ��C�е�ʵ������Ϊ�е���ɫ�������ɣ�װ��C�з�����Ӧ�����ӷ���ʽΪS2-+Cl2�TS��+2Cl-��
�ʴ�Ϊ��Ũ���ᡢKMnO4��Na2S��S2-+Cl2�TS��+2Cl-��
��5����Ҫ֤���ǽ����ԣ�C��Si������ͨ��������̼�����Ʒ�Ӧ���������ԵĹ�����֤��������B�м�Na2CO3����A�п��Լ����ᣬͨ�������̼���Ƶķ�Ӧ����ȡCO2��Ȼ���CO2ͨ��C�е�Na2SiO3�У����Է�����Ӧ��Na2SiO3+CO2+H2O=H2SiO3��+Na2CO3��������ɫ��״�������Ӷ�����֤�����ԣ�H2CO3��H2SiO3���ʷǽ����ԣ�C��Si��
�ʴ�Ϊ�����Na2SiO3���а�ɫ��״����������
���� ���⿼������ʵ�鷽����ƣ��漰�������ǽ�����ǿ����̽������ȷ���ʵ������ǽⱾ��ؼ���֪�������ԡ��ǽ�����ǿ���жϷ���������������������ʵ�飬��Ŀ�Ѷ��еȣ�

| A�� | Na��O��H | B�� | Na+[��O��H]- | C�� | N����N | D�� | H+[��Cl��]- |
| A�� | ��״���£�1mol�κ��������ʵ������ԼΪ22.4L | |
| B�� | 1mol��������ԼΪ22.4L | |
| C�� | ��״���£�1molO2��N2�����������ȣ������ԼΪ22.4L | |
| D�� | �κ������£������Ħ���������22.4L |
| ��ѧ�� | C-C | C-H | H-H | C-O | C=O | H-O |
| ����/kJ•mol-1 | 348 | 413 | 436 | 358 | 750 | 463 |
| ��ѧ�� | H-H | Cl-Cl | H-Cl |
| ���� | 436 | 243 | 431 |