题目内容
18.广阔的海洋蕴藏着丰富的化学资源,含有几十种元素,下列属于海水中微量元素的是( )| A. | 氧 | B. | 钠 | C. | 碘 | D. | 氢 |
分析 海水中含有多种元素,其中Cl、Na、H、O等量较高属于常量元素,碘的含量很小,属于微量元素.
解答 解:广阔的海洋蕴藏着丰富的化学资源,含有几十种元素,其中O、Na、H的含量较高属于常量元素,碘的含量很小,属于微量元素,属于属于海水中微量元素的是碘,
故C正确;
故选C.
点评 本题考查了海水中常见元素含量的判断,属于基础知识的考查,题目难度不大.

练习册系列答案
相关题目
6.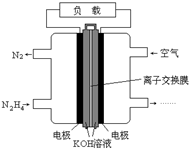 液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述正确的是( )
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述正确的是( )
 液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述正确的是( )
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述正确的是( )| A. | 电子从右侧电极经过负载后流向左侧电极 | |
| B. | 负极发生的电极反应式为:N2H4-4e-=N2+4H+ | |
| C. | 该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 | |
| D. | 该燃料电池持续放电时.K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜 |
13.甲、乙、丙、丁分别是BaCl2、NaOH、FeCl2、Al2(SO4)3、四种物质中的一种.若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,丁溶液滴入甲溶液时,无明显现象发生.据此可推断丙物质是( )
| A. | BaCl2 | B. | NaOH | C. | FeCl2 | D. | Al2(SO4)3 |
3.下列各组离子能够在指定环境下大量共存的是( )
| A. | 在pH=0的溶液中:Na+、K+、MnO4-、Cl- | |
| B. | 和Al反应能产生H2的溶液:K+、NH4+、Cl-、S2O32- | |
| C. | 中性溶液:Al3+、K+、SO42-、AlO2- | |
| D. | c(H+)<c(OH-)的溶液:Na+、K+、SO32-、S2- |
13.高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O$?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
| A. | 放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2 | |
| B. | 充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O | |
| C. | 放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 | |
| D. | 放电时正极附近溶液的碱性减弱 |
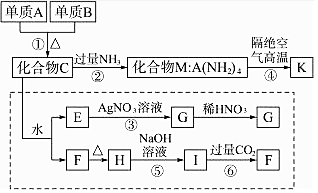 材料科学是近年来与化学有关的科学研究的重点,某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化等特性,它是以中学化学中的常见物质为原料来生产的.如图所示为其生产过程,其中虚线框内转化是为探究C的组成而设.已知A、B均为非金属单质,G、F、H均难溶于水且为白色粉末;图中除M、K(均含A元素)外均为中学化学常见物质:
材料科学是近年来与化学有关的科学研究的重点,某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化等特性,它是以中学化学中的常见物质为原料来生产的.如图所示为其生产过程,其中虚线框内转化是为探究C的组成而设.已知A、B均为非金属单质,G、F、H均难溶于水且为白色粉末;图中除M、K(均含A元素)外均为中学化学常见物质:
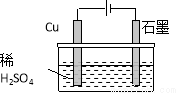
 CuSO4+H2↑
CuSO4+H2↑