题目内容
碳酸钠与100mL某浓度的盐酸恰好完全反应后得到气体5.6L(标准状况).试求:
(1)碳酸钠的物质的量.
(2)所用盐酸的物质的量浓度.
(1)碳酸钠的物质的量.
(2)所用盐酸的物质的量浓度.
考点:化学方程式的有关计算
专题:
分析:发生Na2CO3+2HCl=2NaCl+H2O+CO2↑,n(CO2)=
=0.25mol,结合反应及c=
计算.
| 5.6L |
| 22.4L/mol |
| n |
| V |
解答:
解:(1)n(CO2)=
=0.25mol,由Na2CO3+2HCl=2NaCl+H2O+CO2↑可知,碳酸钠的物质的量为0.25mol,
答:碳酸钠的物质的量为0.25mol;
(2)由反应可知n(HCl)=0.25mol×2=0.5mol,则所用盐酸的物质的量浓度为
=5mol/L,
答:所用盐酸的物质的量浓度为5mol/L.
| 5.6L |
| 22.4L/mol |
答:碳酸钠的物质的量为0.25mol;
(2)由反应可知n(HCl)=0.25mol×2=0.5mol,则所用盐酸的物质的量浓度为
| 0.5mol |
| 0.1L |
答:所用盐酸的物质的量浓度为5mol/L.
点评:本题考查化学反应方程式的计算,为高频考点,把握发生的反应及物质的量关系为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
随着核电荷数的递增,氧化性逐渐减弱的一组是( )
| A、I2、Br2、Cl2、F2 |
| B、F2、Cl2、Br2、I2 |
| C、F-、Cl-、Br-、I- |
| D、Li、Na、K、Rb |
在Na2SO4和Al2(SO4)3的混合溶液中,测得Al3+浓度为0.1mol/L,加入等体积0.3mol/L的BaCl2溶液恰好使SO42-完全沉淀,则混合溶液中Na+的浓度为( )
| A、0.3 mol/L |
| B、0.45 mol/L |
| C、0.6 mol/L |
| D、0.15 mol/L |
电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH--2e-═ZnO+H2O:Ag2O+H2O+2e-═2Ag+2OH-.总反应式为:Ag2O+Zn═2Ag+ZnO,下列说法正确的是( )
| A、Zn为正极,Ag2O为负极 |
| B、电解质溶液中,OH-移向Ag2O极 |
| C、原电池工作时,正极区溶液pH值增大 |
| D、原电池工作时,负极区溶液pH值增大 |
向含溶质0.2mol的Al2(SO4)3溶液中加入1000mL KOH溶液,生成白色沉淀7.8g,则KOH溶液的物质的量浓度可能为( )
| A、0.3mol/L |
| B、0.7mol/L |
| C、0.8 mol/L |
| D、1.5mol/L |
两种气态烃组成的混合气体,其平均组成为C2H3,分析混合气体的成分和体积比( )
| A、V(C2H2):V(C2H4)=1:1 |
| B、V(C2H2):V(C2H6)=3:1 |
| C、V(C2H4):V(C2H6)=2:1 |
| D、V(C2H2):V(C2H6)=1:3 |
 +Zn→CH2=CH2+ZnBr2.写出以1,3-丁二烯为原料合成高分子化合物
+Zn→CH2=CH2+ZnBr2.写出以1,3-丁二烯为原料合成高分子化合物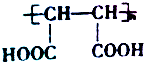 的流程图.
的流程图.