题目内容
下列各组物质中,化学键类型完全相同的是( )
A. 和 和 | B. 和 和 | C. 和 和 | D. 和 和 |
B
解析试题分析:A、HI中化学键为共价键,NaI中化学键为离子键,化学键类型不相同;B、H2S中化学键为极性共价键,CO2中化学键为极性共价键,化学键类型相同;C、Cl2中化学键为非极性共价键,CCl4中化学键为极性共价键,化学键类型不相同;D、F2中化学键为共价键,NaBr中化学键为离子键,化学键类型不相同。
考点:本题考查化学键类型的判断。

 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案(15分)(1)碳、氮、氧的第一电离能大小顺序为 ,氧原子电子排布式为 。
(2)氨分子氮原子杂化类型 ,氨水中四种氢键哪一种是主要的 ,规律是什么? 。画出氢氟酸溶液中最主要氢键 。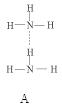
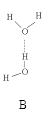
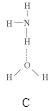
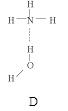
(3)DNA中四种碱基间通过氢键可能的配对方式,用虚线把氢键表示出来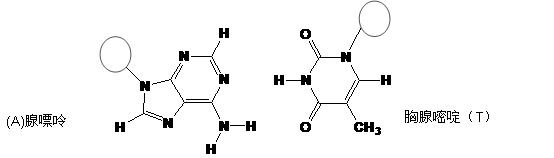

(4)试分析富马酸的K2大于其顺式异构体马来酸K2的原因。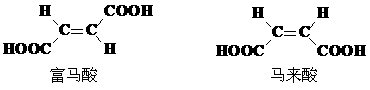
(5)下表是三种火箭推进剂的沸点,为什么火箭推进剂选择氮元素? 。
| 物质 | H2 | N2H4 | H2NN(CH3)2 |
| 沸点/℃ | -252.8 | 113.5 | ~116 |
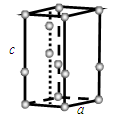
回答下列问题:
①计算晶胞中含有几个水分子。 ②计算冰的密度。
近期《美国化学会志》报道,中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、80MPa下合成出金刚石,具有深远意义。下列说法不正确的是( )
| A.由二氧化碳合成金刚石是化学变化 | B.金刚石是碳的一种同位素 |
| C.钠被氧化最终生成碳酸钠 | D.金刚石中只含有非极性共价键 |
氯化溴(BrCl)结构和性质类似Br2、Cl2。下列叙述正确的是
| A.BrCl是离子化合物 | B.Br-Cl键长大于Cl-Cl键长 |
| C.BrCl 和Br2中都存在极性键 | D.BrCl和Cl2都是非极性分子 |
下表物质与其所含化学键类型、所属化合物类型完全正确的一组是
| 选 项 | A | B | C | D |
| 物 质 | CO2 | MgCl2 | HCl | NaOH |
| 所含化学键类型 | 共价键 | 离子键、共价键 | 离子键 | 离子键、共价键 |
| 所属化合物类型 | 共价化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
N2中含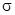 键和
键和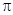 键的数目分别为
键的数目分别为
| A.1,1 | B.2,2 | C.1,2 | D.2,1 |
下列说法正确的是
①离子化合物含离子键,也可能含极性键或非极性键②共价化合物含共价键,也可能含离子键
③含金属元素的化合物不一定是离子化合物 ④由非金属元素组成的化合物一定是共价化合物
⑤由分子构成的物质中一定存在共价键 ⑥熔融状态能导电的化合物是离子化合物
| A.①③⑥ | B.②④⑥ | C.②③④ | D.①③⑤ |
电子数相等的微粒叫做等电子体,下列各组微粒属于等电子体是
| A.CO和CO2 | B.NO和CO | C.CH4和NH3 | D.OH- 和S2- |