题目内容
下表物质与其所含化学键类型、所属化合物类型完全正确的一组是
| 选 项 | A | B | C | D |
| 物 质 | CO2 | MgCl2 | HCl | NaOH |
| 所含化学键类型 | 共价键 | 离子键、共价键 | 离子键 | 离子键、共价键 |
| 所属化合物类型 | 共价化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
A
解析试题分析:A. CO2是共价化合物,含有共价键,正确;B.MgCl2只含离子键,是离子化合物,错误;C.HCl含有共价键,是根据化合物,错误;D.NaOH含有离子键、共价键,是离子化合物,错误。
考点:考查物质与其所含化学键类型、所属化合物类型的关系的知识。

练习册系列答案
相关题目
( 13分)下面的表格是元素周期表的一部分,其中的字母对应不同的元素。
| A | | | |||||||||||||||
| | | | | M | Q | R | | | |||||||||
| | | E | | | | D | | ||||||||||
| | | | G | | | | J | | | | | | | | | | |
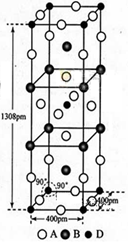
(1)G和J形成的合金是一种贮氢材料,其晶体结构与氯化铯相同。该合金中每个G原子周围与其最近且等距的J原子有 个。该晶体属于 晶体
A .离子晶体 B . 原子晶体 C . 分子晶体 D. 金属晶体
(2)M3R2是一种直线型分子R=M=M=M=R,该分子是一种 分子(填极性或非极性)。
(3)请写出D-的电子排布式: 。
(4)M2A2也是直线型分子,1个分子中含有 个σ键。
(5)化合物E2D6分子中各原子均达到了八电子稳定结构,请画出其结构式。(用元素符号表示)
下列各含氧酸中,酸性最强的是
| A.HMnO4 | B.H2SeO3 | C.H3BO3 | D.H3PO4 |
下列各组物质中,化学键类型完全相同的是( )
A.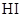 和 和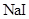 | B.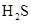 和 和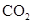 | C.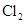 和 和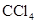 | D.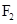 和 和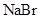 |
下列分子或离子中,含有孤对电子的是
A.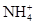 | B.CH4 | C.H2S | D.SiH4 |
关于化学键的各种叙述中正确的是( )
| A.在离子化合物里,只存在离子键 | B.非极性键只存在于双原子的单质分子里 |
| C.共价化合物里,一定不存在离子键 | D.不同元素组成的多原子分子里,只存在极性键 |
含有极性键的共价化合物是
| A.Na2O2 | B.NaOH | C.H2 | D.HC1 |
下列物质的分子中既有σ键又有π键的是( )
①HCl ②H2O ③N2 ④H2O2 ⑤C2H4 ⑥C2H2
| A.①②③ | B.③④⑤⑥ | C.①③⑥ | D.③⑤⑥ |