题目内容
4.下列各组离子能够大量共存的是( )| A. | pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42- | |
| B. | 在含大量Al3+的溶液中:Na+、K+、AlO2-、NO3- | |
| C. | 滴入甲基橙指示剂呈红色的溶液中:Na+、NH4+、CO32-、NO3- | |
| D. | 水电离出的c(H+)=1×10-13mol•L-1的溶液中:K+、HCO3-、Cl-、NH4+ |
分析 A.pH=0的溶液,显酸性;
B.离子之间相互促进水解;
C.滴入甲基橙指示剂呈红色的溶液,显酸性;
D.水电离出的c(H+)=1×10-13mol•L-1的溶液,为酸或碱溶液.
解答 解:A.pH=0的溶液,显酸性,该组离子之间不反应,可大量共存,故A正确;
B.AlO2-、Al3+相互促进水解,不能大量共存,故B错误;
C.滴入甲基橙指示剂呈红色的溶液,显酸性,不能大量存在CO32-,故C错误;
D.水电离出的c(H+)=1×10-13mol•L-1的溶液,为酸或碱溶液,酸溶液中不能大量存在HCO3-,碱溶液中不能大量存在HCO3-、NH4+,故D错误;
故选A.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、水解反应的离子共存考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.把少量废铁屑溶于过量的稀硫酸中,过滤,除去杂质,在滤液中加入适量的硝酸,再加入过量的氨水,有红褐色沉淀生成.过滤,加热至沉淀物质量不再变化,得到红棕色的残渣.上述沉淀和残渣分别为( )
| A. | Fe(OH)3;Fe2O3 | B. | Fe(OH)2;FeO | ||
| C. | Fe(OH)3Fe(OH)2;Fe2O3 | D. | Fe2O3;Fe(OH)3 |
12.有X、Y、Z、W四种主族元素,若已知阳离子X、Y和阴离子Z、W具有相同的电子层结构,并且离子径X>Y、Z>W,则四种元素的原子序数为( )
| A. | W>Y>Z>X | B. | Y>X>W>Z | C. | Y>X>Z>W | D. | Z>Y>X>W |
9.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1mol•L-1K2SO4溶液中含有钾离子数为2NA | |
| B. | 0.1mol铁与0.1mol氯气点燃完全反应,转移电子数为0.3NA | |
| C. | 常温常压下,6.4g氧气和臭氧混合气体中含有的原子总数为0.4NA | |
| D. | 1L1mol•L-1氨水中,含有的NH3与NH3•H20分子的总数为NA |
4.除去下列物质中含有的少量杂质(括号中的物质)的方法,错误的是( )
| A. | NH4Cl溶液(I2)用CCl4萃取 | B. | NO(NH3)通过水洗涤 | ||
| C. | NaCl(NH4Cl)加热固体混合物 | D. | N2(NO2)通过水洗涤 |
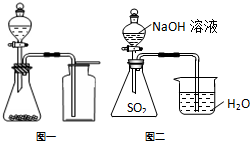
5.下列说法中正确的是 ( )

| A. | 氯气通入澄清石灰水中,制取漂白粉 | |
| B. | 可通过化合反应得到Fe(OH)3 | |
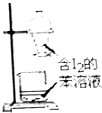
| C. | 选择合适的试剂,用图一所示装置可分别制取少量CO2、NO和O2 | |
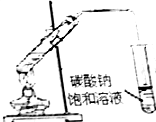
| D. | 用图二的装置可证明SO2与NaOH发生了化学反应 |
 金属及其化合物在化学中扮演着重要的角色,同学们应该熟练掌握它们的性质.
金属及其化合物在化学中扮演着重要的角色,同学们应该熟练掌握它们的性质.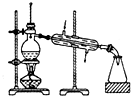
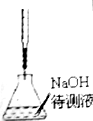
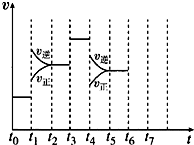 在一密闭容器中发生反应N2+3H2?2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
在一密闭容器中发生反应N2+3H2?2NH3,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示: