题目内容
11.手性化合物一般是指含手性碳原子的化合物,手性碳原子是指连接有四个不同的原子或原子团的碳原子.化合物CH3-CH2-CH(OH)-CH=CH2中含有一个手性碳原子,则下列变化中不能使该手性化合物的手性消失的是( )| A. | 氧化反应 | B. | 取代反应 | C. | 加成反应 | D. | 消去反应 |
分析 该有机物含有羟基,可发生氧化反应、取代反应、消去反应,含有醛基,可发生加成和氧化反应,结合手性碳原子的定义解答该题;
解答 解:A.化合物CH3-CH2-CH(OH)-CH=CH2中羟基被氧化,得到化合物CH3-CH2-$\stackrel{\stackrel{O}{∥}}{C}$-CH=CH2,不含手性碳原子,故A不选;
B.化合物CH3-CH2-CH(OH)-CH=CH2中羟基与HBr发生取代反应,得到化合物CH3-CH2-CHBr-CH=CH2,含手性碳原子,故B选;
C.化合物CH3-CH2-CH(OH)-CH=CH2中 C=C与氢气发生加成反应,得到化合物CH3-CH2-CH(OH)-CH2CH3,不含手性碳原子,故C不选;
D.化合物CH3-CH2-CH(OH)-CH=CH2中羟基发生消去反应,得到化合物CH3-CH=CH-CH=CH2,不含手性碳原子,故D不选;
故选B.
点评 本题考查有机物的结构和性质,题目难度不大,注意把握手性碳原子的定义和官能团的性质为解答该题的关键.

练习册系列答案
相关题目
6.某硫酸铝溶液中,含 Al3+ a g,则溶液中 SO42- 的物质的量为( )
| A. | $\frac{3a}{2}$ mol | B. | $\frac{a}{18}$ mol | C. | $\frac{a}{27}$ mol | D. | $\frac{a}{96}$ mol |
16.SO2随意排放会造成严重的大气污染.下列是某小组同学设计处理烟气(主要含SO2、N2、O2、粉尘)中SO2的方法.
(1)方法一:利用氯碱工业产品处理SO2的烟气,流程如下:
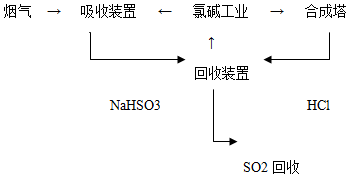
①“吸收装置”中发生反应的离子方程式SO2+OH-=HSO3-.
②合成塔中每合成1mol气体放出热量92.3kJ(25℃、101kPa),反应的热化学方程式H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ•mol-1.
③上述流程中循环利用的物质是NaCl溶液.
(2)方法二:利用FeCl3溶液氧化吸收烟气中SO2
①该反应的离子方程式2Fe3++SO2+2H2O=2Fe2++SO42-+4H+(反应a).为验证该反应,同学们将SO2通入0.05mol/LFeCl3溶液中,溶液很快由黄色变为红褐色;将溶液长时间放置后,最终变为浅绿色.关于红褐色液体,以下是同学们的分析推测与实验.
②利用胶体的丁达尔效应(填性质)可以检验步骤I中是否得到了Fe(OH)3胶体.
③根据反应b说明步骤II中液体颜色变化的原因是加入铁粉时发生反应2Fe3++Fe=3Fe2+,c(Fe3+)减小,使反应b逆向移动(用离子方程式及必要的文字说明).
(1)方法一:利用氯碱工业产品处理SO2的烟气,流程如下:

①“吸收装置”中发生反应的离子方程式SO2+OH-=HSO3-.
②合成塔中每合成1mol气体放出热量92.3kJ(25℃、101kPa),反应的热化学方程式H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ•mol-1.
③上述流程中循环利用的物质是NaCl溶液.
(2)方法二:利用FeCl3溶液氧化吸收烟气中SO2
①该反应的离子方程式2Fe3++SO2+2H2O=2Fe2++SO42-+4H+(反应a).为验证该反应,同学们将SO2通入0.05mol/LFeCl3溶液中,溶液很快由黄色变为红褐色;将溶液长时间放置后,最终变为浅绿色.关于红褐色液体,以下是同学们的分析推测与实验.
| 分析推测 | 实验步骤及现象 |
| 甲:生成了Fe(OH)3胶体 乙:经查阅资料,可能发生反应: Fe3++6SO2?Fe(SO2)63+(反应b) | I、制备Fe(OH)3胶体并检验 II、分别向Fe(OH)3胶体和该红褐色液体中加入适量铁粉,振荡后前者不变色,后者变为浅绿色 |
③根据反应b说明步骤II中液体颜色变化的原因是加入铁粉时发生反应2Fe3++Fe=3Fe2+,c(Fe3+)减小,使反应b逆向移动(用离子方程式及必要的文字说明).
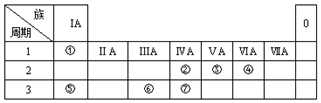
1.在以下性质的比较中,正确的是( )
| A. | 微粒半径:Li+<O2-<F-<Na+ | B. | 电负性:F>N>O>C | ||
| C. | 分子中的键角:CO2>H2O>CH4>NH3 | D. | 共价键的键能:H-F>H-Cl>H-Br>H-I |
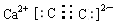 ,乙是一种常用的还原剂,请用化学方程式表示它在工业上的一种重要用途:3CO+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2.
,乙是一种常用的还原剂,请用化学方程式表示它在工业上的一种重要用途:3CO+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3CO2. .
.