题目内容
8.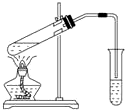 下列实验能获得成功的是( )
下列实验能获得成功的是( )| A. | 用如图所示装置,无水乙酸和乙醇共热制取乙酸乙酯 | |
| B. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复原来的红色 | |
| C. | 水和乙醇的混合液,可用蒸馏的方法使其分离 | |
| D. | 淀粉用酸催化水解后的溶液加入新制银氨溶液,水浴加热,可观察到有银镜出现 |
分析 A.需要浓硫酸作催化剂、吸水剂;
B.铜丝在酒精灯上加热后生成CuO,CuO可氧化乙醇;
C.水和乙醇的混合液互溶,但沸点不同,直接蒸馏易形成共沸混合物;
D.淀粉水解生成葡萄糖,检验葡萄糖应在碱性条件下.
解答 解:A.用如图所示装置,试管中乙醇、浓硫酸、无水乙酸共热制取乙酸乙酯,故A错误;
B.铜丝在酒精灯上加热后生成CuO,CuO可氧化乙醇,则立即伸入无水乙醇中,CuO与乙醇反应生成乙醛、Cu和水,铜丝恢复原来的红色,故B正确;
C.水和乙醇的混合液互溶,但沸点不同,直接蒸馏易形成共沸混合物,则应加CaO后再用蒸馏的方法使其分离,故C错误;
D.淀粉水解生成葡萄糖,检验葡萄糖应在碱性条件下,则水解后,先加碱至碱性,再加入新制银氨溶液,水浴加热,观察是否有银镜出现,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握有机物的性质、有机物的制备、混合物分离提纯等为解答的关键,侧重分析与实验能力的考查,注意有机物性质及实验的结合及实验评价性分析,题目难度不大.

练习册系列答案
相关题目
18.在醋酸中存在电离平衡:CH3COOH?CH3COO-+H+,要使电离平衡右移且溶液中c(OH-)增大,应采取的措施是( )
| A. | 加入醋酸钠固体 | B. | 加入盐酸 | C. | 加入蒸馏水 | D. | 升高温度 |
16.有一瓶Na2SO3溶液,由于它可能部分被氧化,某同学进行如下实验:取少量溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀.对此实验下述结论正确的是( )
| A. | Na2SO3已部分被空气中的氧气氧化 | |
| B. | 加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4 | |
| C. | 题中操作可证明Na2SO3溶液是否被氧化 | |
| D. | 此实验不能确定Na2SO3是否部分被氧化 |
3.下列关于各实验装置的叙述中,正确的是( )


| A. | ①装置可用于蒸干氯化铝溶液制AlCl3 | |
| B. | ②装置可用于分离CCl4萃取碘水后已分层的有机层和水层 | |
| C. | ③装置可用于收集NH3或HCl气体,并防止倒吸 | |
| D. | ④装置盐桥中的K+自右向左移动 |
13.将1molCH4和适量的O2在密闭容器中点燃,充分反应后,CH4和O2均无剩余,且产物均为气体(101kPa,120℃),总质量为72g,下列有关叙述不正确的是( )
| A. | 若将产物通过碱石灰,则不能被完全吸收 | |
| B. | 若将产物通过浓硫酸,充分吸收后,浓硫酸增重18g | |
| C. | 产物的平均摩尔质量为24g.mol-1 | |
| D. | 反应中消耗O256g |
20.下列物质的分子中,所有的原子都在同一平面上的是( )
| A. | NH3 | B. | C2H6 | C. | 甲烷 | D. | 乙烯 |
17.将4mol A气体和2mol B气体在1L的容器中混合,并在一定条件下发生如下反应:2A(g)+B(g)?2C(g),若是2min后测得A的浓度为2mol/L,物质A表示的反应速率正确的是( )
| A. | 2mol/L•min | B. | 1 mol/L•min | C. | 0.5 mol/L•min | D. | 0.6 mol/L•min |
18.下列说法中正确的是( )
| A. | 烃是指含有碳、氢元素的有机物 | |
| B. | 燃烧后能产生CO2和H2O的有机物一定是烃 | |
| C. | 天然气、沼气、坑气、煤气的主要成分都是甲烷 | |
| D. | 形成化合物种类最多的元素位于周期表中第二周期第IVA族 |
 ,A分子中最多在同一平面的原子数为16;
,A分子中最多在同一平面的原子数为16;

 +H2O→
+H2O→


 .
.