题目内容
19.某含苯环的化合物A,且除苯环外没有其它环,其相对分子质量为104,碳的质量分数为92.3%.(1)A的结构简式为
 ,A分子中最多在同一平面的原子数为16;
,A分子中最多在同一平面的原子数为16;(2)A与其它有机物有以下转化关系,D的分子式为C8H6O2,请回答以下问题:

①经测定E中含有氯元素,E的结构简式是

②写出B+H2O→C的化学方程式
 +H2O→
+H2O→
③D的结构简式是

(3)已知:

请写出A与稀、冷的KMnO4溶液在碱性条件下反应产物的结构简式
 .
.
分析 烃A的相对分子质量为104,碳的质量分数为92.3%,则分子中碳原子数目为$\frac{104×92.3%}{12}$=8,故氢原子数目为$\frac{104-12×8}{1}$=8,A的分子式为C8H8,分子中除苯环外没有其它环,则A的结构简式为 ,A发生氧化反应生成B,B与水反应生成C,C在浓硫酸作用是得到B,C发生催化氧化生成D的分子式为C8H6O2,可推知B为
,A发生氧化反应生成B,B与水反应生成C,C在浓硫酸作用是得到B,C发生催化氧化生成D的分子式为C8H6O2,可推知B为 ,C为
,C为 ,D为
,D为 ,A与稀氯水反应、B与HCl反应均生成E,且E中含有氯元素,则E
,A与稀氯水反应、B与HCl反应均生成E,且E中含有氯元素,则E .
.
解答 解:烃A的相对分子质量为104,碳的质量分数为92.3%,则分子中碳原子数目为$\frac{104×92.3%}{12}$=8,故氢原子数目为$\frac{104-12×8}{1}$=8,A的分子式为C8H8,分子中除苯环外没有其它环,则A的结构简式为 ,A发生氧化反应生成B,B与水反应生成C,C在浓硫酸作用是得到B,C发生催化氧化生成D的分子式为C8H6O2,可推知B为
,A发生氧化反应生成B,B与水反应生成C,C在浓硫酸作用是得到B,C发生催化氧化生成D的分子式为C8H6O2,可推知B为 ,C为
,C为 ,D为
,D为 ,A与稀氯水反应、B与HCl反应均生成E,且E中含有氯元素,则E
,A与稀氯水反应、B与HCl反应均生成E,且E中含有氯元素,则E .
.
(1)A的结构简式为: ,旋转碳碳单键可以使苯环与碳碳双键的平面共面,分子中所有原子都可以共面,A分子中最多在同一平面的原子数为16,
,旋转碳碳单键可以使苯环与碳碳双键的平面共面,分子中所有原子都可以共面,A分子中最多在同一平面的原子数为16,
故答案为: ;16;
;16;
(2)①E的结构简式是: ,故答案为:
,故答案为: ;
;
②B+H2O→C的化学方程式: +H2O→
+H2O→ ,
,
故答案为: +H2O→
+H2O→ ;
;
③D的结构简式是: ,故答案为:
,故答案为: ;
;
(3)反应的方程式为: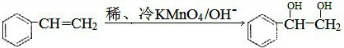 ,
,
故答案为: .
.
点评 本题考查有机物的推断,A的结构的确定是推断的关键,再利用正推法与逆推法相结合推断其它物质,侧重考查学生分析推理能力,是对有机物知识的综合运用,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9. 某化学兴趣小组要完成中和热的测定.
某化学兴趣小组要完成中和热的测定.
(1)实验仪器、药品:
实验桌上备有大、小两个烧杯、温度计、泡沫塑料、泡沫塑料板、胶头滴管、0.50mol•L-1盐酸、0.55mol•L-1NaOH溶液,实验尚缺少的玻璃用品是环形玻璃棒搅拌、量筒;
(2)实验原理:
该小组用50mL0.50mol/L的盐酸和50mL0.55mol/L的NaOH溶液,在组装好的装置中进行中和反应,并通过 测定反应过程中所放出的热量计算中和热.
(3)实验数据如下:
已知:中和热计算公式为△H=-$\frac{(4.18×1{0}^{-3})•{m}_{总}•({t}_{2}-{t}_{1})}{n({H}_{2}O)}$kJ•mol-1
①表中t1为氢氧化钠溶液和盐酸的初始温度的平均值,则t2的意义是
反应后的最高温度.
②根据公式,计算实验结果后写出NaOH溶液与HCl溶液反应的热化学方程式HCl(aq)+NaOH(aq)=NaCl(aq)+2H2O(l)△H=-56.848kJ•mol-1.
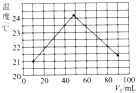
③实验过程中始终保持V1(氢氧化钠溶液)+V2(盐酸)=100mL.测量并记录溶液温度如图所示.
分析该图象得出如下两点结论:
酸碱中和反应为放热反应;做该实验时环境温度低于21℃(填“高于”“等于”或“低于”).
(4)相关误差分析
a.中和热测定的实验,测量结果偏高的原因可能是C(填选项字母).
A.由于大小烧杯间空隙过大,填充了很多的泡沫塑料
B.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
C.量取NaOH溶液的体积时仰视读数
D.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
b.若改用60mL0.50mol/L盐酸跟50mL0.55mol/L的NaOH溶液进行反应,从理论上说所求中和热相等(填“相等”或“不相等”);若用醋酸代替HCl做实验,对测定结果有(填“有”或“无”)影响.
 某化学兴趣小组要完成中和热的测定.
某化学兴趣小组要完成中和热的测定.(1)实验仪器、药品:
实验桌上备有大、小两个烧杯、温度计、泡沫塑料、泡沫塑料板、胶头滴管、0.50mol•L-1盐酸、0.55mol•L-1NaOH溶液,实验尚缺少的玻璃用品是环形玻璃棒搅拌、量筒;
(2)实验原理:
该小组用50mL0.50mol/L的盐酸和50mL0.55mol/L的NaOH溶液,在组装好的装置中进行中和反应,并通过 测定反应过程中所放出的热量计算中和热.
(3)实验数据如下:
| 实验编号 | 实验用品 | 溶液温度 | 中和热 | |
| t2-t1 | △H | |||
| ① | 50mL0.55mol•L-1NaOH溶液 | 50mL0.50mol•L-1盐酸 | 3.3℃ | ? |
| ② | 50mL0.55mol•L-1NaOH溶液 | 50mL0.50mol•L-1盐酸 | 3.5℃ | |
①表中t1为氢氧化钠溶液和盐酸的初始温度的平均值,则t2的意义是
反应后的最高温度.
②根据公式,计算实验结果后写出NaOH溶液与HCl溶液反应的热化学方程式HCl(aq)+NaOH(aq)=NaCl(aq)+2H2O(l)△H=-56.848kJ•mol-1.
③实验过程中始终保持V1(氢氧化钠溶液)+V2(盐酸)=100mL.测量并记录溶液温度如图所示.
分析该图象得出如下两点结论:
酸碱中和反应为放热反应;做该实验时环境温度低于21℃(填“高于”“等于”或“低于”).
(4)相关误差分析
a.中和热测定的实验,测量结果偏高的原因可能是C(填选项字母).
A.由于大小烧杯间空隙过大,填充了很多的泡沫塑料
B.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
C.量取NaOH溶液的体积时仰视读数
D.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
b.若改用60mL0.50mol/L盐酸跟50mL0.55mol/L的NaOH溶液进行反应,从理论上说所求中和热相等(填“相等”或“不相等”);若用醋酸代替HCl做实验,对测定结果有(填“有”或“无”)影响.
10.表是元素周期表的一部分,其中每个数字序号代表一种短周期元素.
请按要求回答下列问题:
(1)元素②在周期表中的位置为第二周期第IVA族
(2)④、⑤两种元素相比较,金属性强的是Na(填元素符号);
(3)这些元素的最高价氧化物对应水化物中酸性最强的是HClO4(填化学式,下同),具有两性的是Al(OH)3.
(4)元素④和元素⑥形成的化合物的电子式为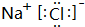 .
.
(5)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式HCl+NH3═NH4Cl.
| ① | ||||||||
| ② | ③ | |||||||
| ④ | ⑤ | ⑥ | ||||||
(1)元素②在周期表中的位置为第二周期第IVA族
(2)④、⑤两种元素相比较,金属性强的是Na(填元素符号);
(3)这些元素的最高价氧化物对应水化物中酸性最强的是HClO4(填化学式,下同),具有两性的是Al(OH)3.
(4)元素④和元素⑥形成的化合物的电子式为
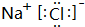 .
.(5)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式HCl+NH3═NH4Cl.
14.苯与乙烯相比较,下列叙述不正确的是( )
| A. | 都能在空气中燃烧 | |
| B. | 都容易发生取代反应 | |
| C. | 苯和乙烯都能在一定条件下发生加成反应 | |
| D. | 苯不能使酸性KMnO4溶液褪色而乙烯能 |
11.关于下列一组图示的说法中正确的是( )
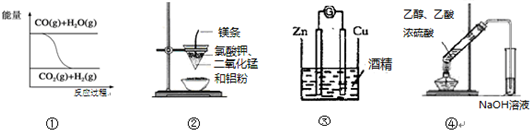

| A. | 图①表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”为吸热反应 | |
| B. | 图②可以制取金属锰 | |
| C. | 图③形成原电池 | |
| D. | 图④制取乙酸乙酯 |
8.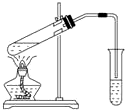 下列实验能获得成功的是( )
下列实验能获得成功的是( )
 下列实验能获得成功的是( )
下列实验能获得成功的是( )| A. | 用如图所示装置,无水乙酸和乙醇共热制取乙酸乙酯 | |
| B. | 将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复原来的红色 | |
| C. | 水和乙醇的混合液,可用蒸馏的方法使其分离 | |
| D. | 淀粉用酸催化水解后的溶液加入新制银氨溶液,水浴加热,可观察到有银镜出现 |
9.苯的结构式可用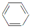 来表示,下列关于苯的叙述中正确的是( )
来表示,下列关于苯的叙述中正确的是( )
 来表示,下列关于苯的叙述中正确的是( )
来表示,下列关于苯的叙述中正确的是( )| A. | 苯是无色无味,密度比水大的液体 | |
| B. | 苯中含有碳碳双键,所以苯属于烯烃 | |
| C. | 苯分子中6个碳碳化学键完全相同 | |
| D. | 苯可以与溴水、高锰酸钾溶液反应而使它们褪色 |
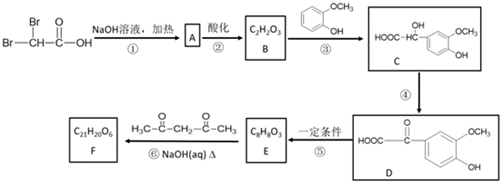
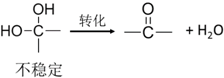

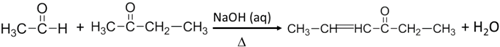
 .反应④的化学方程式是
.反应④的化学方程式是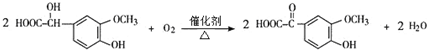 .
.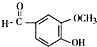 .F的结构简式是
.F的结构简式是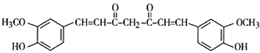 .
.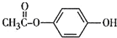 .
.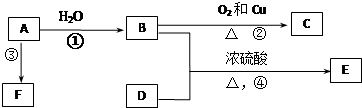
 ,该反应类型是取代反应.
,该反应类型是取代反应.