题目内容
6.下列有机物中,属于烃的衍生物且含有两种官能团的是( )| A. | CH3Cl | B. | CH3CH2OH | C. | CH2═CHBr | D. | CH2=CH2 |
分析 烃的衍生物可看成烃中H被其它原子或原子团取代后的产物,常见的有机物的官能团为碳碳双键、三键、-OH、-CHO、-COOH、-COOC-、-X等,以此来解答.
解答 解:A.含官能团为-Cl,故A不选;
B.含官能团为-OH,故B不选;
C.含官能团为碳碳双键、-Br,含C、H、Br元素,属于烃的衍生物且含有两种官能团,故C选;
D.官能团为碳碳双键,故D不选;
故选C.
点评 本题考查有机物的官能团,为高频考点,把握常见官能团的判断为解答的关键,侧重分析与应用能力的考查,注意烃的衍生物判断,题目难度不大.

练习册系列答案
相关题目
5.下列溶液中微粒的物质的量浓度关系不正确的是( )
| A. | 将0.1molCl2全部溶于水形成的1L溶液中:2c(Cl2)+c(Cl-)+c(HClO)+c(ClO-)=0.2mol•L-1 | |
| B. | Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+c(H2CO3) | |
| C. | 物质的量浓度均为0.1mol•L-1的NaClO与NaHCO3的混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) | |
| D. | 室温下,向0.01mol•L-1的NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
14.恒温、恒压下,在一个容积可变的容器中发生如下反应:N2+3H2?2NH3
(1)若开始时放入1mol N2和3mol H2,达到平衡后,生成a mol NH3
(2)若开始时无NH3,只放入N2和H2,达到平衡时生成NH3的物质的量为3a mol,则开始时放入N2和H2的物质的量分别为( )
(1)若开始时放入1mol N2和3mol H2,达到平衡后,生成a mol NH3
(2)若开始时无NH3,只放入N2和H2,达到平衡时生成NH3的物质的量为3a mol,则开始时放入N2和H2的物质的量分别为( )
| A. | 1mol和9mol | B. | 2mol和9mol | C. | 3mol和9mol | D. | 3mol和6mol |
1.Na2FeO4(Fe为+6价)是一种高效多功能水处理剂,应用前景十分看好.一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,(已知Na2O2中O为-1价)对此反应下列说法中正确的是( )
| A. | Na2O2只作氧化剂,O2是还原产物 | |
| B. | Na2FeO4既是氧化产物又是还原产物 | |
| C. | 由上述方程式可知氧化性:Na2FeO4>Na2O2>O2 | |
| D. | 2 mol FeSO4发生反应时,反应中共有8 mol电子转移 |
18.下列说法正确的是( )
| A. | 投入铁片产生H2的溶液中可大量存在H+、Mg2+、SO42-、NO3- | |
| B. | 无色溶液中可能大量存在Al3+、NH4+、Cl-、S2- | |
| C. | 1.0 mol•L-1的KNO3溶液中可大量存在H+、Fe2+、Cl-、SO42- | |
| D. | 弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- |
16.下列溶液中物质的量浓度为1mol•L-1的是( )
| A. | 将40g NaOH溶解于1L水中 | |
| B. | 将22.4L氯化氢气体溶于水配成1L溶液 | |
| C. | 从100mL 10mol•L-1的浓盐酸中取出10mL | |
| D. | 20g NaOH溶解在水中配成500mL溶液 |
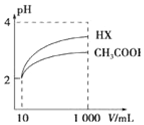 物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种.请根据所学化学知识回答下列问题:
物质在水溶液中可能存在电离平衡、盐的水解平衡或沉淀溶解平衡,它们都可看作化学平衡的一种.请根据所学化学知识回答下列问题: