题目内容
17. 科学家合成了具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关说法不正确的是( )
科学家合成了具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关说法不正确的是( )| A. | Al2H6中铝的杂化方式为sp3杂化 | |
| B. | 氢铝化合物可能成为未来的储氢材料和火箭燃料 | |
| C. | Al2H6中含有离子键和极性共价键 | |
| D. | Al2H6在空气中完全燃烧,产物为三氧化二铝和水 |
分析 A、铝原子形成4个σ键;
B、根据氢铝化合物组成元素为Al和H两种元素,而Al和H2都是很好的燃料,但氢气的在储存盒运输中是极不方便,将其转化成氢铝化合物后,就解决这一矛盾,同时氢铝化合物的燃烧热极高因此可以作为未来的储氢材料和火箭燃料;
C、Al2H6为分子晶体,化合物中Al和H之间为共价键;
D、根据元素守恒分析解答.
解答 解:A、铝原子形成4个σ键,所以Al2H6中铝的杂化方式为sp3杂化,故A正确;
B、根据氢铝化合物组成元素为Al和H两种元素,而Al和H2都是很好的燃料,但氢气的在储存盒运输中是极不方便,将其转化成氢铝化合物后,就解决这一矛盾,同时氢铝化合物的燃烧热极高因此可以作为未来的储氢材料和火箭燃料,故B正确;
C、Al2H6为分子晶体,化合物中Al和H之间为共价键,无离子键,故C错误;
D、根据元素守恒可知Al2H6在空气中完全燃烧,产物为三氧化二铝和水,故D正确;
故选C.
点评 本题考查了元素化合物的性质在实际中的应用,属于知识应用的问题,解决这类问题,需要将知识点与题中的信息有机的结合起来,解决时需分析清楚题意,要细心认真.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.一定量的稀硫酸与足量的镁反应,为了加快反应速率又不影响氢气的总量,可采取的措施为( )
| A. | 加压 | B. | 加CuCl2固体 | C. | 加NaCl溶液 | D. | 加醋酸钠固体 |
8.下列叙述中,正确的是( )
| A. | 将一小块金属钠投入稀硫酸铜溶液中会有红色固体析出 | |
| B. | 向0.4mol浓盐酸中加入足量的MnO2,加热,可收集(标准状况下)2.24LCl2 | |
| C. | 向足量的盐酸和氢氧化钠溶液中各加入等质量的Al粉,消耗盐酸与氢氧化钠溶液的物质的量之比为3:1 | |
| D. | 150 mL 1 mol•L-1NaCl溶液与75 mL 1 mol•L-1 Na2CO3溶液中Na+物质的量浓度相等 |
5.表为元素周期表的一部分(数字为原子序数),其中X为35的是( )
| A. |
| B. |
| C. |
| D. |
|
12.关于元素周期表的说法正确的是( )
| A. | 第三周期有8种元素 | |
| B. | 短周期元素是指第一、二周期所含有的全部元素 | |
| C. | 元素周期表有8个主族 | |
| D. | IA族中的元素全部是金属元素 |
2.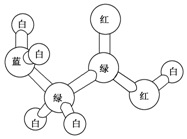 某期刊封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图可代表一种( )
某期刊封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图可代表一种( )
 某期刊封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图可代表一种( )
某期刊封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图可代表一种( )| A. | 卤代羧酸 | B. | 酯 | C. | 氨基酸 | D. | 乙醇钠 |
6.我国可燃冰的开采技术领先世界,关于可燃冰的说法正确的是( )
| A. | 可燃冰可能在未来汽车“燃油”替变为“燃冰” | |
| B. | 可燃冰即使开采不当也不会造成“温室效应” | |
| C. | 可燃冰中有一种甲烷气体,甲烷属无机物 | |
| D. | 可燃冰中的乙醚与乙醇互为同分异构体 |
13.物质的性质决定其用途.下列说法正确的是( )
| A. | 二氧化氯具有强氧化性,可用来漂白织物 | |
| B. | 氯化铝是强电解质,可电解其水溶液获得金属铝 | |
| C. | 石英坩埚耐高温,可用来加热熔化烧碱、纯碱等固体 | |
| D. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |