题目内容
2.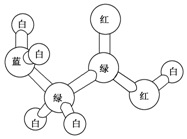 某期刊封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图可代表一种( )
某期刊封面上有如下一个分子的球棍模型图,图中“棍”代表单键或双键或三键.不同颜色的球代表不同元素的原子,该模型图可代表一种( )| A. | 卤代羧酸 | B. | 酯 | C. | 氨基酸 | D. | 乙醇钠 |
分析 根据不同颜色代表不同的元素,先判断含有的元素种类,再根据原子的成键类型判断元素,从而确定该物质的类型,以此解答该题.
解答 解:由原子成键特点知:白球为氢原子、蓝球为氮原子、绿球为碳原子、红球为氧原子,则该有机物的结构简式为: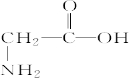 ,应为氨基酸,故选:C
,应为氨基酸,故选:C
点评 本题考查有机物的结构,为高频考点,把握有机物的结构中C原子的成键、官能团及分类为解答的关键,侧重分析与应用能力的考查,注意球表示的原子种类,题目难度不大

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
10.下列物质与水混合后,显著放热的是( )
| A. | 生石灰 | B. | 无水乙醇 | C. | 浓硫酸 | D. | 固体硝酸铵 |
17. 科学家合成了具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关说法不正确的是( )
科学家合成了具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关说法不正确的是( )
 科学家合成了具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关说法不正确的是( )
科学家合成了具有独特化学特性的氢铝化合物(AlH3)n.已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高.Al2H6球棍模型如图.下列有关说法不正确的是( )| A. | Al2H6中铝的杂化方式为sp3杂化 | |
| B. | 氢铝化合物可能成为未来的储氢材料和火箭燃料 | |
| C. | Al2H6中含有离子键和极性共价键 | |
| D. | Al2H6在空气中完全燃烧,产物为三氧化二铝和水 |
7.下列说法正确的是( )
| A. | 离子化合物中只能含有离子键 | |
| B. | 化学反应的过程,本质上是旧化学键断裂和新化学键形成的过程 | |
| C. | 化学键存在于分子之间 | |
| D. | 共价化合物中可能含有离子键 |
18.孔雀石的主要成分是Cu2(OH)2CO3(含Fe2O3、FeCO3、Al2O3、SiO2杂质),工业上用孔雀石制备硫酸铜的第一步需用过量的硫酸溶解并过滤.常温下,分别取滤液并向其中加入指定物质,反应后的溶液中大量存在的一组离子正确的是( )
| A. | 加入过量氨水:Fe3+、NH4+、SO42-、OH- | |
| B. | 加入过量NaClO溶液:Fe2+、H+、Cu2+、SO42- | |
| C. | 加入过量NaOH溶液:Na+、AlO2-、SO42-、OH- | |
| D. | 加入过量NaHCO3溶液:Na+、Al3+、SO42-、HCO3- |

 铬及其化合物广泛应用于生活、生产.酒精测量仪的原理是:
铬及其化合物广泛应用于生活、生产.酒精测量仪的原理是: .
.