题目内容
常温时,将500mLpH=a的CuSO4和K2SO4的混合溶液用石墨电极电解一段时间,测得溶液的pH变为b(假设溶液体积的变化忽略不计),在整个电解过程中始终发现只有一个电极有气体产生.下列说法不正确的是( )
| A、若使溶液恢复到电解前的浓度可以向溶液中加20(10-b-10-a)g CuO |
| B、b<a<7 |
| C、阳极电极反应:4OH--4e-═2O2↑+4H+ |
| D、整个过程中是阳极产生氧气,阴极析出铜单质 |
考点:电解原理
专题:电化学专题
分析:根据题意分析,在整个电解过程中始终只有一个电极上有气体产生,所以电解池工作时,阳极上氢氧根离子放电,生成氧气;阴极上铜离子得电子生成铜单质,所以电池反应式为2CuSO4+2H2O
2H2SO4+2Cu+O2↑,电解后生成硫酸的物质的量=(10-b-10-a)mol/L×
×0.5L=0.25(10-b-10-a)mol.
| ||
| 1 |
| 2 |
解答:
解:A、要使溶液恢复到原来的浓度,应向电解后的溶液中加入电解时析出的物质,即氧化铜或者碳酸铜,质量为0.25(10-b-10-a)×124=31(10-b-10-a) g CuCO3,故A错误;
B、电解时,阳极上氢氧根离子放电,阴极上铜离子放电,所以导致溶液中氢离子浓度越来越大,溶液的PH值越来越小,即b<a<7,故B正确;
C、电解时,阳极上溶液中氢氧根离子失电子发生氧化反应电极反应:4OH--4e-═2O2↑+4H+,故C正确;
D、电解时,阴极上溶液中铜离子得电子发生还原反应,电极反应式为Cu2++2e-=Cu,结合C阳极生成氧气,故D正确.
故选A.
B、电解时,阳极上氢氧根离子放电,阴极上铜离子放电,所以导致溶液中氢离子浓度越来越大,溶液的PH值越来越小,即b<a<7,故B正确;
C、电解时,阳极上溶液中氢氧根离子失电子发生氧化反应电极反应:4OH--4e-═2O2↑+4H+,故C正确;
D、电解时,阴极上溶液中铜离子得电子发生还原反应,电极反应式为Cu2++2e-=Cu,结合C阳极生成氧气,故D正确.
故选A.
点评:本题以电解原理为载体考查了氧化还原反应的有关计算,难度较大,明确溶液中离子的放电顺序是解本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
关于图中各装置的叙述不正确的是( )


| A、装置①是中和滴定法测定硫酸的物质的量浓度 |
| B、装置②中手捂烧瓶(橡胶管已被弹簧夹夹紧),发现导管中有液柱上升并保持稳定,则说明装置不漏气 |
| C、装置③中X若为四氯化碳,可用于吸收氨气,并防止倒吸 |
| D、装置④证明铁生锈过程中空气参与反应 |
下列叙述正确的是( )
| A、乙烯和苯都能使溴水褪色,褪色的原因相同 |
| B、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| C、乙烯和乙烷都能发生加聚反应 |
| D、石油的裂解是物理变化 |
下列叙述正确的是( )
| A、自然界中大量存在硅单质 |
| B、石英、水晶、硅石的主要成分都是SiO2 |
| C、自然界中SiO2都存在于石英矿中 |
| D、SiO2表示一个二氧化硅分子由一个硅原子和两个氧原子组成 |
分子式为C7H8O的芳香化合物中,与FeCl3溶液混合显紫色和不显紫色的物质分别有( )
| A、2种和1种 |
| B、2种和3种 |
| C、3种和2种 |
| D、3种和1种 |
下列事实不属于盐类水解应用的是( )
| A、明矾、氯化铁晶体常用于净水或消毒 |
| B、实验室通常使用热的纯碱溶液去除油污 |
| C、实验室配制FeCl3溶液时加入少量稀盐酸 |
| D、实验室制氢气时加入CuSO4可加快反应速率 |
如图为雾霾的主要成分示意图.下列说法不正确的是( )
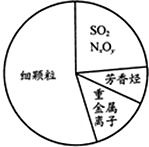

| A、重金属离子可导致蛋白质变性 |
| B、苯是最简单的芳香烃 |
| C、SO2和NxOy都属于酸性氧化物 |
| D、汽车尾气的大量排放是造成雾霾天气的人为因素之一 |
下列有关实验的叙述中,合理的是( )
| A、用25mL碱式滴定管准确量取22.00 mL的KMnO4溶液 |
| B、用广泛pH试纸测出某盐酸溶液的pH为3.2 |
| C、使用pH试纸测定溶液pH时先润湿,则测得溶液的pH都偏小 |
| D、实验室配制氯化铁溶液时,可以先将氯化铁溶解在盐酸中,再配制到所需要的浓度 |