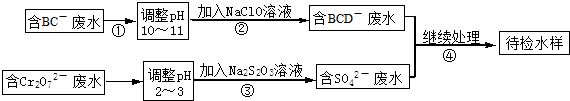
题目内容
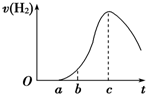 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:(1)该反应若使用催化剂,可使H2产量增多吗?
(2)铝片与硫酸反应产生氢气的离子方程式为
(3)曲线由O→a段不产生氢气的原因是
(4)曲线b→c段,产生氢气的速率增加较快的主要原因是
(5)曲线由c以后,产生氢气的速率逐渐下降的主要原因是
考点:化学反应速率的影响因素
专题:
分析:(1)催化剂加快反应速率,不影响氢气的产量;
(2)铝与硫酸反应生成硫酸铝和氢气;
(3)铝是活泼性较强的金属,能迅速和空气中的氧气反应生成氧化铝,根据氧化铝的性质分析;
(4)金属和酸的反应是放热反应,温度升高是影响反应速率的主要因素,根据温度对化学反应速率的影响分析;
(5)溶液的浓度是影响化学反应速率的主要因素.
(2)铝与硫酸反应生成硫酸铝和氢气;
(3)铝是活泼性较强的金属,能迅速和空气中的氧气反应生成氧化铝,根据氧化铝的性质分析;
(4)金属和酸的反应是放热反应,温度升高是影响反应速率的主要因素,根据温度对化学反应速率的影响分析;
(5)溶液的浓度是影响化学反应速率的主要因素.
解答:
解:(1)催化剂加快反应速率,不影响氢气的产量,故答案为:不会;
(2)铝能够与硫酸中的氢离子反应生成铝离子和氢气,离子方程式为:2Al+6H+═2Al3++3H2↑,故答案为:2Al+6H+═2Al3++3H2↑;
(3)铝是活泼性较强的金属,能迅速和空气中的氧气反应生成氧化铝,氧化铝首先稀硫酸反应生成氯化铝和水,不产生H2,离子方程式为Al2O3+6H+=2Al3++3H2O;
故答案为:硫酸首先与铝片表面的Al2O3反应,不产生H2; Al2O3+3H2SO4=2Al2(SO4)3+3H2O;
(4)金属和酸的反应是放热反应,使溶液的温度升高,温度升高是影响反应速率的主要因素,化学反应速率加快,
故答案为:反应放热,温度升高是影响反应速率的主要因素,使反应速率增大;
(5)随着反应的进行,溶液中的氢离子浓度逐渐降低,氢离子浓度是影响化学反应速率的主要因素,所以反应速率逐渐减小;
故答案为:硫酸的浓度逐渐减小,该因素变为影响化学反应速率的主要因素,化学反应速率开始下降.
(2)铝能够与硫酸中的氢离子反应生成铝离子和氢气,离子方程式为:2Al+6H+═2Al3++3H2↑,故答案为:2Al+6H+═2Al3++3H2↑;
(3)铝是活泼性较强的金属,能迅速和空气中的氧气反应生成氧化铝,氧化铝首先稀硫酸反应生成氯化铝和水,不产生H2,离子方程式为Al2O3+6H+=2Al3++3H2O;
故答案为:硫酸首先与铝片表面的Al2O3反应,不产生H2; Al2O3+3H2SO4=2Al2(SO4)3+3H2O;
(4)金属和酸的反应是放热反应,使溶液的温度升高,温度升高是影响反应速率的主要因素,化学反应速率加快,
故答案为:反应放热,温度升高是影响反应速率的主要因素,使反应速率增大;
(5)随着反应的进行,溶液中的氢离子浓度逐渐降低,氢离子浓度是影响化学反应速率的主要因素,所以反应速率逐渐减小;
故答案为:硫酸的浓度逐渐减小,该因素变为影响化学反应速率的主要因素,化学反应速率开始下降.
点评:本题考查了化学反应速率的影响因素,难度不大,注意根据图象分析理解随反应进行影响反应速率的主要因素,掌握基础是关键.

练习册系列答案
相关题目
下面关于硅的叙述牛,正确的是( )
| A、硅的非金属性比碳强,只有在高温下才能跟氢气起化合反应 |
| B、硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位 |
| C、硅的化学性质不活泼,在自然界中可以以游离态存在 |
| D、硅在电子工业中是重要的半导体材料 |
用蘸有浓氨水的玻璃棒靠近下列各浓酸时,均有白烟产生的一组是( )
| A、H2SO4、HNO3 |
| B、HCl、HNO3 |
| C、HCl、H2SiO3、 |
| D、HCl、H2SO4 |
铝可与硝酸钠发生反应(未配平):Al+NaNO3+H2O→Al(OH)3+N2↑+NaAlO2,有关叙述正确的是( )
| A、上述反应中水是氧化剂 |
| B、若反应过程中转移5 mol e-则生成标准状况下N2的体积为11.2L |
| C、该反应的氧化产物是N2 |
| D、当消耗1 mol Al时,生成标况下N2的体积为22.4L |
人们在研究金星大气成分,发现金星大气中有一种称之为硫化羟(COS)的分子,其结构与CO2类似,硫化羟是一种与生命密切相关的物质.下列有关COS的推测肯定不正确的是( )
| A、COS属于离子化合物 |
| B、COS分子中,所有原子都满足8电子的稳定结构 |
| C、COS的结构式为O=C-S |
| D、COS含有共价键 |
原子核内有6个质子、6个中子的碳原子的质量是1.993×10-26kg,某种原子的质量是9.288×10-26kg,则该原子的相对原子质量是( )
A、
| ||
B、1.993×
| ||
C、
| ||
D、9.288×
|
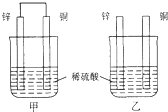 原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.
原电池原理的发现是储能和供能技术的巨大进步,是化学对人类的一项重大贡献.